多选题 适中0.65 引用1 组卷217
H2S是一种剧毒气体,对H2S废气资源化利用的途径之一是回收能量并得到单质硫,反应原理为2H2S(g)+O2(g)=S2(s)+2H2O(l) ΔH=-632 kJ·mol-1.如图为质子膜H2S燃料电池的示意图。下列说法正确的是
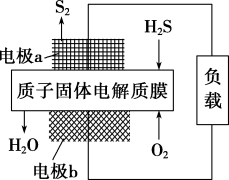

| A.电池工作时,电流从电极a经过负载流向电极b |
| B.电极a上的电极反应式为2H2S-4e-=S2↓+4H+ |
| C.当通入11.2 L O2,转移电子数2NA |
| D.当电路中通过4 mol电子时,有4 mol H+经质子膜进入正极区 |
21-22高二上·山东济南·阶段练习
类题推荐
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l)  H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是
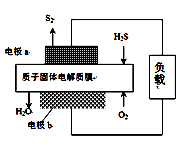
 H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是
| A.电路中每流过2mol电子,电池内部释放316kJ热能 |
| B.每34gH2S参与反应,有2mol H+经质子膜进入正极区 |
| C.电极a为电池的负极 |
D.电极b上发生的电极反应为:O2+4e +4 H+=2H2O +4 H+=2H2O |
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为: 2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ/mol。如图为质子膜H2S燃料电池的示意图。下列说法正确的是( )


| A.电极a为电池的正极 |
| B.电极b上发生的电极反应为:O2+2H2O+4e-=4OH- |
| C.电路中每流过4mol电子,电池内部释放632kJ热能 |
| D.每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) +O2(g ) ===S2 (s)+2H2O(l) △H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是
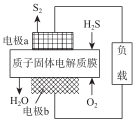

| A.电极a为电池的正极 |
| B.电极 b 上发生的电极反应为:O2+4H+ +4e-===2H2O |
| C.该装置是一种将热能转化为电能的装置 |
| D.H+经质子膜进入a极区 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


