解答题-工业流程题 较易0.85 引用1 组卷341
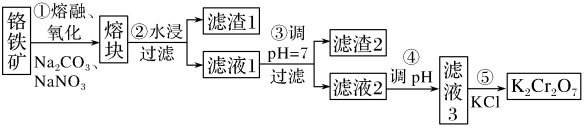
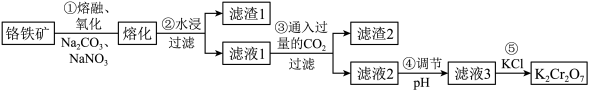
K2Cr2O7是一种重要的化工原料。以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3等杂质)为原料制备K2Cr2O7的一种工艺流程如下:
已知:(a)Cr2O +H2O
+H2O 2CrO
2CrO +2H+
+2H+
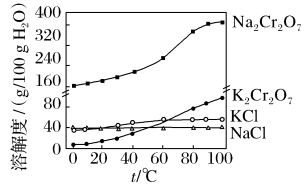
(b)不同温度下各物质的溶解度:
(c)步骤①的主要反应为:2FeO·Cr2O3+4Na2CO3+7NaNO3 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
(1)“滤渣1”和“滤渣2”的主要成分分别是___________ 、___________ (填化学式)。写出步骤③的离子反应方程式___________ ;步骤④中调pH,以下试剂可选用___________ (填标号)。
a.NH3 B.KOH C.CH3COOH D.HCl
(2)在步骤⑤中加入适量KCl,___________ ,过滤得到K2Cr2O7固体。
(3)某工厂用a kg铬铁矿粉(含Cr2O3 40%)制K2Cr2O7,最终得到产品b kg,产率为___________ ×100%(列计算式)。
(4)化学还原法可除去废水中的Cr2O ,取含Cr2O
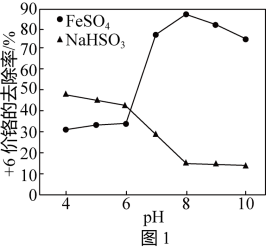
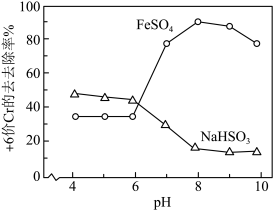
,取含Cr2O 的模拟水样在不同pH条件下,分别向每个水样中加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图所示。
的模拟水样在不同pH条件下,分别向每个水样中加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图所示。
①在酸性条件下,NaHSO3使Cr2O 还原为Cr3+,请写出NaHSO3与Cr2O
还原为Cr3+,请写出NaHSO3与Cr2O 反应的离子方程式:
反应的离子方程式:___________ 。
②pH>8时,亚铁盐对+6价Cr的去除效果反而下降,可能的原因是:___________ 。

已知:(a)Cr2O
(b)不同温度下各物质的溶解度:
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g H2O) | 0 ℃ | 28 | 35.7 | 4.7 | 163 |
| 40 ℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80 ℃ | 51.3 | 38 | 70 | 376 | |
(1)“滤渣1”和“滤渣2”的主要成分分别是
a.NH3 B.KOH C.CH3COOH D.HCl
(2)在步骤⑤中加入适量KCl,
(3)某工厂用a kg铬铁矿粉(含Cr2O3 40%)制K2Cr2O7,最终得到产品b kg,产率为
(4)化学还原法可除去废水中的Cr2O

①在酸性条件下,NaHSO3使Cr2O
②pH>8时,亚铁盐对+6价Cr的去除效果反而下降,可能的原因是:
21-22高三上·山东济南·阶段练习
类题推荐
K2Cr2O7是一种重要的化工原料。以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3等杂质)为原料制备K2Cr2O7的一种工艺流程如下:

(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+O2=Na2CrO4+Fe2O3+CO2(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)“滤渣1”的主要成分为_______ (填化学式),它的一种用途为:_______ 。
(3)依据流程图分析熔融反应时,Al2O3变成_______ (填化学式),写出步骤③的离子反应方程式_______ ;
(4)步骤④中调pH,以实现2CrO +2H+⇌Cr2O
+2H+⇌Cr2O +H2O。以下试剂可选用_______(填标号)。
+H2O。以下试剂可选用_______(填标号)。
(5)在步骤⑤中加入适量KCl可得到K2Cr2O7晶体。已知不同温度下各物质的溶解度:
为使K2Cr2O7晶体充分析出并分离,应采取的操作为_______ 、_______ 、洗涤、干燥。
(6)某工厂用50.0kg铬铁矿粉(含Cr2O338%)制K2Cr2O7,最终得到产品29.4kg,产率为_______ 。

(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+O2=Na2CrO4+Fe2O3+CO2(未配平),该反应中氧化剂与还原剂的物质的量之比为
(2)“滤渣1”的主要成分为
(3)依据流程图分析熔融反应时,Al2O3变成
(4)步骤④中调pH,以实现2CrO
| A.SO2 | B.H2SO4 | C.NaOH | D.HI |
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100gH2O) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 70 | 376 | |
为使K2Cr2O7晶体充分析出并分离,应采取的操作为
(6)某工厂用50.0kg铬铁矿粉(含Cr2O338%)制K2Cr2O7,最终得到产品29.4kg,产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网