多选题 适中0.65 引用1 组卷149
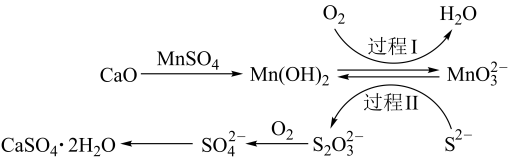
利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的S2-,制取石膏(CaSO4·2H2O)的过程如图所示,下列说法错误的是

| A.CaSO4·2H2O属于盐类和混合物 |
| B.过程Ⅱ中,反应的离子方程式为:4MnO |
| C.过程Ⅰ后溶液pH增大 |
| D.将10 L上清液中的S2-(S2-浓度为480 mg·L-1)转化为SO |
21-22高三上·山东济南·阶段练习
类题推荐
利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的 ,制取石膏(
,制取石膏( )的过程如下:
)的过程如下:

下列说法正确的是

下列说法正确的是
| A. |
| B.过程II中反应的离子方程式为 |
| C.过程I后溶液pH增大 |
| D.将10L上清液中的 |
利用空气催化氧化法除掉电石浆(含CaO)上层清液中的S2-,制取石膏(CaSO4·2H2O)的过程如图。下列说法错误的是

| A.CaSO4·2H2O属于俗称生石膏,属于纯净物 |
| B.过程I中氧化剂与还原剂的物质的量之比为1:2 |
| C.将10L上清液中的S2-(S2-浓度为480 mg·L-1 )转化为 |
| D.过程Ⅱ中,反应的离子方程式为: |
工业上除去电石渣浆(含CaO)上清液中的S2-,并制取石膏的常用流程如图:

下列说法错误的是

下列说法错误的是
| A.石膏的化学式CaSO4∙2H2O |
| B.Mn(OH)2在过程Ⅰ中作还原剂, |
| C.过程Ⅰ和过程Ⅱ的总反应的离子方程式:3O2+4S2-=2 |
| D.10L清液中的S2-(浓度为480mg/L)被O2氧化为 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


