解答题-原理综合题 适中0.65 引用1 组卷30
合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1molN2和1molH2加入刚性容器中充分反应,测得NH3的物质的量分数为4%,其他条件不变,温度升高至450℃,测得NH3的物质的量分数为2.5%,则可判断合成氨反应△H___ 0(填“ ”或“
”或“ ”)。
”)。
(2)在2L密闭容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
①温度T1___ (填“>”“<”或“=”)T3。
②在T2温度下,达到平衡时N2的转化率为__ 。
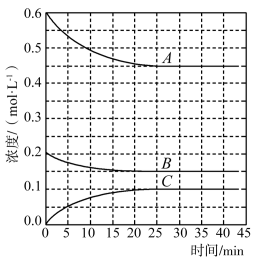
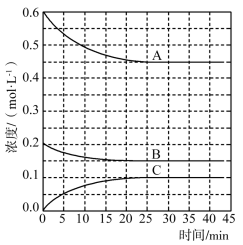
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
①表示H2浓度变化的曲线是___ (填“A”、“B”或“C”。与(1)中的实验条件(1.01×105Pa、450℃)相比,改变的条件可能是___ 。
②在0~25min内N2的平均反应速率为___ 。在该条件下反应的平衡常数为___ (保留两位有效数字)。
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1molN2和1molH2加入刚性容器中充分反应,测得NH3的物质的量分数为4%,其他条件不变,温度升高至450℃,测得NH3的物质的量分数为2.5%,则可判断合成氨反应△H
(2)在2L密闭容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
| 温度/K | T1 | T2 | T3 | T4 |
| n(NH3)/mol | 3.6 | 3.2 | 2.8 | 2.0 |
①温度T1
②在T2温度下,达到平衡时N2的转化率为
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)

①表示H2浓度变化的曲线是
②在0~25min内N2的平均反应速率为
21-22高二上·山东枣庄·阶段练习
类题推荐
合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)在2L密闭绝热容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
①下列能说明该反应已达到平衡状态的是___ 。
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②温度T1___ (填“>”“<”或“=”)T3。
③在T3温度下,达到平衡时N2的体积分数____ 。
(2)N2O4为重要的火箭推进剂之一、N2O4与NO2转换的热化学方程式为N2O4(g) 2NO2(g)△H。上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,则该反应的化学平衡常数Kp为
2NO2(g)△H。上述反应中,正反应速率v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,则该反应的化学平衡常数Kp为___ (以k正、k逆表示)。若将定量N2O4投入真空容器中恒温恒压分解(温度298K、压强110kPa),已知该条件下k逆=5×102kPa-1·s-1,当N2O4分解10%时,v逆=____ kPa·s-1。
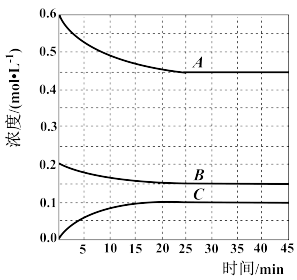
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
①表示H2浓度变化的曲线是____ (填“A”、“B”或“C”。与(1)中的实验条件(1.01×105Pa、450℃)相比,改变的条件可能是___ 。
②在0~25min内N2的平均反应速率为___ 。在该条件下反应的平衡常数为___ mol-2·L2(保留两位有效数字)。
(1)在2L密闭绝热容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
| 温度/K | T1 | T2 | T3 | T4 |
| n(NH3)/mol | 3.6 | 3.2 | 2.8 | 2.0 |
①下列能说明该反应已达到平衡状态的是
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②温度T1
③在T3温度下,达到平衡时N2的体积分数
(2)N2O4为重要的火箭推进剂之一、N2O4与NO2转换的热化学方程式为N2O4(g)
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)

①表示H2浓度变化的曲线是
②在0~25min内N2的平均反应速率为
合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3.在1.01×105 Pa、250 ℃时,将1 mol N2和1 mol H2加入a L刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450 ℃,测得NH3体积分数为0.025,则可判断合成氨反应为_______ (填“吸热”或“放热”)反应。
(2)在1.01×105 Pa、250 ℃时,将2 mol N2和2 mol H2加入a L密闭容器中充分反应,H2平衡转化率可能为_______(填标号)。
(3)我国科学家结合实验与计算机模拟结果,研究了在铁掺杂W18049纳米反应器催化剂表面上实现常温低电位合成氨,获得较高的氨产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
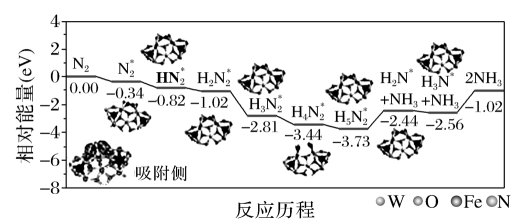
需要吸收能量最大的能垒(活化能)E=_______ eV,该步骤的化学方程式为_______
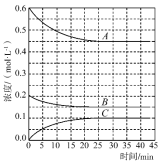
(4)T ℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是
2NH3(g)反应过程中各物质浓度的变化曲线如图所示:表示N2浓度变化的曲线是_______ (填“A”、“B”或“C”)。与(1)中的实验条件(1.01×105 Pa、450 ℃)相比,改变的条件可能是_______ 。
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3.在1.01×105 Pa、250 ℃时,将1 mol N2和1 mol H2加入a L刚性容器中充分反应,测得NH3体积分数为0.04;其他条件不变,温度升高至450 ℃,测得NH3体积分数为0.025,则可判断合成氨反应为
(2)在1.01×105 Pa、250 ℃时,将2 mol N2和2 mol H2加入a L密闭容器中充分反应,H2平衡转化率可能为_______(填标号)。
| A.=4% | B.<4% | C.4%~7% | D.>11.5% |

需要吸收能量最大的能垒(活化能)E=
(4)T ℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网