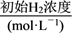解答题-原理综合题 适中0.65 引用2 组卷159
回答问题
(1)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂条件下,使CCl4转化为重要的化工原料氯仿(CHCl3)。在一个固定容积为2 L的密闭容器中发生反应:CCl4(g)+H2(g) CHCl3(g)+HCl(g),达到平衡后,测得实验数据见表:
CHCl3(g)+HCl(g),达到平衡后,测得实验数据见表:
① 请利用“三段式”计算此反应在110 ℃时的平衡常数___________ 。(要求写出详细过程)
② 实验1中CCl4的转化率为___________ 。
③ 判断该反应的正反应是吸热反应还是放热反应,并说明理由。___________ ,理由为___________ 。
(2)向一个2 L的密闭容器中充入7 mol A气体和5 mol B气体,充分混合后在一定条件下反应:3A(g)+B(g) 2C(s)+xD(g),经5 min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.2 mol·(L·min)-1 ,求:
2C(s)+xD(g),经5 min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.2 mol·(L·min)-1 ,求:
①B的转化率___________ ;
②x的值为___________ ;
③平衡时压强与初始时压强之比___________ ;
④此温度下此反应的平衡常数的值为___________ 。
(1)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂条件下,使CCl4转化为重要的化工原料氯仿(CHCl3)。在一个固定容积为2 L的密闭容器中发生反应:CCl4(g)+H2(g)
| 实验序号 | 温度/C | 初始n(CCl4)/mol | 初始n(H2)/mol | 平衡时n(CHCl3)/mol |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
② 实验1中CCl4的转化率为
③ 判断该反应的正反应是吸热反应还是放热反应,并说明理由。
(2)向一个2 L的密闭容器中充入7 mol A气体和5 mol B气体,充分混合后在一定条件下反应:3A(g)+B(g)
①B的转化率
②x的值为
③平衡时压强与初始时压强之比
④此温度下此反应的平衡常数的值为
21-22高二上·福建三明·阶段练习
类题推荐
工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应: ,使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
,使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
(1)此反应在110℃时平衡常数为___________ 。
(2)实验l中,CCl4的转化率为___________ 。
(3)判断该反应的正反应是___________ (填“放热”或“吸热”),理由是___________ 。
(4)为提高实验3中CCl4的转化率,可采取的措施是___________ 。
a.使用高效催化剂
b.向容器中再投入1mol CCl4和1mol H2
c.温度升高到200℃
d.向容器中再投入1mol HCl
e.向容器中再投入1mol H2
| 实验序号 | 温度℃ | 初始n(CCl4)(mol) | 初始n(H2)(mol) | 平衡时n(CHCl3)(mol) |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
(2)实验l中,CCl4的转化率为
(3)判断该反应的正反应是
(4)为提高实验3中CCl4的转化率,可采取的措施是
a.使用高效催化剂
b.向容器中再投入1mol CCl4和1mol H2
c.温度升高到200℃
d.向容器中再投入1mol HCl
e.向容器中再投入1mol H2
甲烷是一种重要的基础化工原料,不仅可制备多种重要有机产品,还可用于环境保护。请回答下列问题:
(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染。已知:

反应过程(2)是__ 反应(填“放热”或“吸热”),甲烷还原NO2生成H2O(g)、N2和CO2时的热化学方程式是__ 。
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应:CCl4(g)+H2(g) CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
①此反应在110℃时平衡常数为___ 。
②实验l中,CCl4的转化率为__ 。
③判断该反应的正反应是__ (填“放热”或“吸热”),理由是__ 。
④为提高实验3中CCl4的转化率,可采取的措施是__ 。
a.使用高效催化剂
b.向容器中再投入1molCCl4和1molH2
c.温度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染。已知:

反应过程(2)是
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应:CCl4(g)+H2(g)
 CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:| 实验 序号 | 温度℃ | 初始n(CCl4)( mol) | 初始n(H2)( mol) | 平衡时n(CHCl3)( mol) |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
①此反应在110℃时平衡常数为
②实验l中,CCl4的转化率为
③判断该反应的正反应是
④为提高实验3中CCl4的转化率,可采取的措施是
a.使用高效催化剂
b.向容器中再投入1molCCl4和1molH2
c.温度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
(1)2molA 1molB在一定条件下反应:2A(g)+B(g) 4C(g) ΔH<0。若①恒温恒容条件下A的体积分数为a%;②恒温恒压条件下A的体积分数为b%;③恒容绝热条件下A的体积分数为c%;则它们之间的关系是(填“>”、“<”或“=”):
4C(g) ΔH<0。若①恒温恒容条件下A的体积分数为a%;②恒温恒压条件下A的体积分数为b%;③恒容绝热条件下A的体积分数为c%;则它们之间的关系是(填“>”、“<”或“=”):______________________
(2)为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂作用下,通过下列反应:CCl4+H2 CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。
CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。
①此反应的化学平衡常数表达式为________________ ,在110 ℃时平衡常数为________ 。
②实验1中,CCl4的转化率A________ 50%(填“大于”、“小于”或“等于”)。
③实验2中,10 h后达到平衡,H2的平均反应速率为________ 。
④已知该反应的熵变为0,实验3中,B的值________ 50%(填“大于”、“小于”、“等于”)。
 4C(g) ΔH<0。若①恒温恒容条件下A的体积分数为a%;②恒温恒压条件下A的体积分数为b%;③恒容绝热条件下A的体积分数为c%;则它们之间的关系是(填“>”、“<”或“=”):
4C(g) ΔH<0。若①恒温恒容条件下A的体积分数为a%;②恒温恒压条件下A的体积分数为b%;③恒容绝热条件下A的体积分数为c%;则它们之间的关系是(填“>”、“<”或“=”):(2)为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化剂作用下,通过下列反应:CCl4+H2
 CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。
CHCl3+HCl使CCl4转化为重要的化工原料氯仿(CHCl3)。此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为77 ℃,CHCl3的沸点为61.2 ℃。在密闭容器中,该反应达到平衡状态后,测得如下数据(假设不考虑副反应)。实验序号 | 温度℃ | 初始CCl4浓度/(mol·L-1) |
| CCl4的平衡转化率 |
1 | 110 | 0.8 | 1.2 | A |
2 | 110 | 1 | 1 | 50% |
3 | 100 | 1 | 1 | B |
②实验1中,CCl4的转化率A
③实验2中,10 h后达到平衡,H2的平均反应速率为
④已知该反应的熵变为0,实验3中,B的值
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网