填空题 适中0.65 引用1 组卷174
完成下列问题。
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入___________ 。(“+”或“−”)
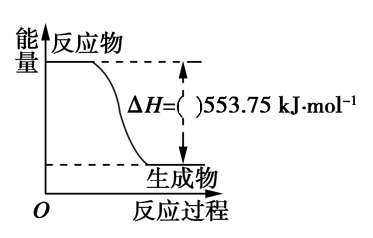
②写出表示丙烷燃烧热的热化学方程式:___________ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___________ 。
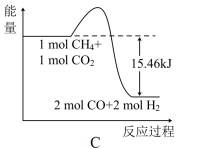
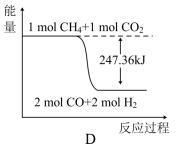
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为___________ (用阿伏加德罗常数NA表示),放出的热量为___________ kJ。
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1___________ ΔH2
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1___________ ΔH2
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+ O2(g)=CO(g) ΔH2<0,则ΔH1
O2(g)=CO(g) ΔH2<0,则ΔH1___________ ΔH2
(1)第十四届运动会于2021年9月15日在西安奥体中心体育场隆重开幕,00”后体坛新秀杨倩,带着我们共同的希望和梦想,点燃主火炬。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,图中的括号内应该填入

②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2生成N2,反应中转移的电子总数为
(3)反应热大小比较(填“>”“<”或“=”)
A(g)+B(g)=C(g) ΔH1<0;A(g)+B(g)=C(l) ΔH2<0,则ΔH1
S(g)+O2(g)=SO2(g) ΔH1<0;S(s)+O2(g)=SO2(g) ΔH2<0,则ΔH1
C(s)+O2(g)=CO2(g) ΔH1<0;C(s)+
21-22高二上·甘肃白银·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网