解答题-原理综合题 适中0.65 引用1 组卷76
为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
(1)实验①的目的是___ 。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是____ (用实验中所提供的几种试剂)。
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:
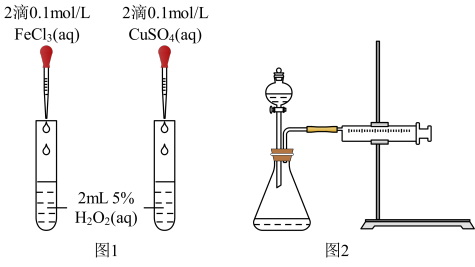
①定性分析:如图1可通过观察____ ,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是___ 。
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是___ 。
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
①实验结果表明,催化剂的催化效果与___ 有关。
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因___ 。
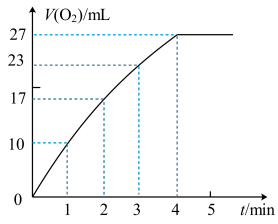
| 编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入3滴FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡;试管B中产生的气泡量增多 |
| ② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液 | 两支试管中均未明显见到有气泡产生 |
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图所示的实验。请回答相关问题:

①定性分析:如图1可通过观察
②定量分析:用图2所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(4)MnO2对H2O2分解反应也有催化作用,另一个同学用图2装置,将状态不同的1gMnO2分别加入盛有30mL等浓度的H2O2溶液的锥形瓶中,产生气体进入注射器针筒中,记录结果如下:
| MnO2状态 | 触摸锥形瓶情况 | 该温度下针筒内收集到气体的体积 | 所需时间 |
| 粉末状 | 很烫 | 30mL | 3min |
| 块状 | 微热 | 30mL | 9min |
②实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因
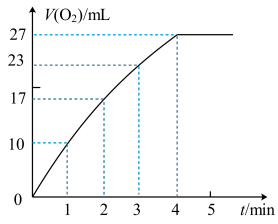
21-22高二上·福建龙岩·阶段练习
类题推荐
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
(1)过氧化氢分解的化学方程式为_______ 。
(2)实验①的目的是_______ 。实验中滴加FeCl3溶液的目的是_______ 。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______ (用实验中所提供的几种试剂)。
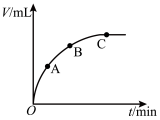
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是_______ 。

| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡;试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5 mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生。 |
(2)实验①的目的是
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是

为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
(1)实验①的目的是________________________________________ ,实验中滴加 溶液的目的是
溶液的目的是______________________________________________ 。
(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是________________________________________________ (用实验中所提供的试剂和仪器)。
(3)某同学在50mL一定浓度的 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是
溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是______________ 。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL5% | 试管A中不再产生气泡,试管B中产生气泡的量增大 |
| ② | 另取两支试管分别加入5mL5% | 两试管中均未明显见到有气泡产生 |
(2)实验②中未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出对上述操作的改进意见是
(3)某同学在50mL一定浓度的

H2O2被称为绿色氧化剂,对其性质进行研究极其重要。
I.某市售H2O2溶液中含H2O2的质量分数为30%,密度1.11g/ml, 回答下列问题。
(1)该市售双氧水溶液中H2O2的物质的量浓度_______ 。(结果保留2位小数)
II.某同学以H2O2分解为例,按照下表探究温度、浓度、催化剂、酸对反应速率的影响。
(2)在实验①和②中,H2O2分解速率较快的是_______ ,设计实验②和③的目的是_______ ;
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出的实验结论是_______ 。

III.如图另一个同学将状态不同的1gMnO2分别加入盛有30 mL等浓度的H2O2溶液的锥形瓶中

产生气体进入注射器针筒中,记录结果如下:
(4)锥形瓶中发生反应的化学方程式_______ ,装置a的名称_______ ,实验结果表明,催化剂的催化效果与_______ 有关。
(5)实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因_______ 。

I.某市售H2O2溶液中含H2O2的质量分数为30%,密度1.11g/ml, 回答下列问题。
(1)该市售双氧水溶液中H2O2的物质的量浓度
II.某同学以H2O2分解为例,按照下表探究温度、浓度、催化剂、酸对反应速率的影响。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20 mL 2% H2O2溶液+2 mL H2O | 无 | 20℃ |
| ② | 20 mL 5% H2O2溶液+2 mL H2O | 无 | 20℃ |
| ③ | 20 mL 5% H2O2溶液+2 mL H2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20 mL 5% H2O2溶液+2 mL 1 mol/L HCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20 mL5% H2O2溶液+2 mLH2O | 1g粉末状MnO2 | 40℃ |
(2)在实验①和②中,H2O2分解速率较快的是
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出的实验结论是

III.如图另一个同学将状态不同的1gMnO2分别加入盛有30 mL等浓度的H2O2溶液的锥形瓶中

产生气体进入注射器针筒中,记录结果如下:
| MnO2状态 | 触摸锥形瓶情况 | 该温度下针筒内收集到气体的体积 | 所需时间 |
| 粉末状 | 很烫 | 30mL | 3 min |
| 块状 | 微热 | 30mL | 9 min |
(4)锥形瓶中发生反应的化学方程式
(5)实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


