解答题-工业流程题 适中0.65 引用2 组卷187
I.铁、铝是生活中常见金属,用途广泛。完成下列填空:
(1)在碱性溶液中,Al(OH)3的电离方程式为:___________ 。
(2)铝和氧化铁高温下反应得到的熔融物通常为铁铝合金,设计实验证明其含金属铝_____ 。
II.高铁酸钾 是一种集氧化、杀菌、吸附、凝聚等新型多功能高效水处理剂。
是一种集氧化、杀菌、吸附、凝聚等新型多功能高效水处理剂。 在水中发生发如下反应生成具有很强氧化、杀菌能力的新生态氧原子(用
在水中发生发如下反应生成具有很强氧化、杀菌能力的新生态氧原子(用 表示):___________
表示):___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(3)配平上述反应_______ 。此过程中氧化剂是_________ 。(填化学物质)。
(4) 本身不具有吸附性,作为水处理剂为何具有吸附、凝聚等功能?
本身不具有吸附性,作为水处理剂为何具有吸附、凝聚等功能?_______ 。
III.溶液在工业上用于蚀刻铜箔制造电路板。从蚀刻后的废液中可以回收铜并使蚀刻液再生,流程如下(部分物质有省略):
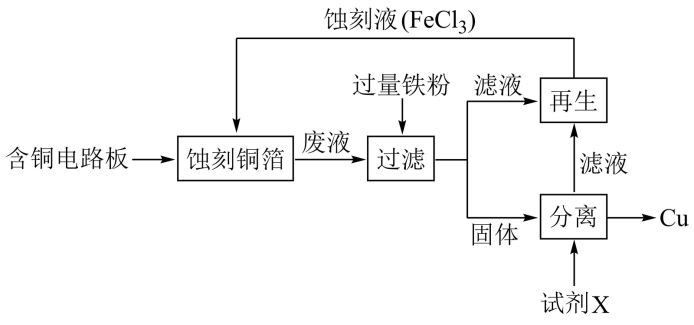
(5) 蚀刻铜箔反应的离子方程式为
蚀刻铜箔反应的离子方程式为___________ 。
(6)从固体中分离出铜,加入的试剂X可以是___________ 。
(7)使滤液再生为蚀刻液可采用的方法是___________ 。
(1)在碱性溶液中,Al(OH)3的电离方程式为:
(2)铝和氧化铁高温下反应得到的熔融物通常为铁铝合金,设计实验证明其含金属铝
II.高铁酸钾
(3)配平上述反应
(4)
III.溶液在工业上用于蚀刻铜箔制造电路板。从蚀刻后的废液中可以回收铜并使蚀刻液再生,流程如下(部分物质有省略):

(5)
(6)从固体中分离出铜,加入的试剂X可以是
(7)使滤液再生为蚀刻液可采用的方法是
20-21高二上·上海杨浦·阶段练习
类题推荐
铁是人类较早使用的金属之一,完成下列问题。
(1)下列铁的化合物中,可以由单质直接化合得到的是___________(用字母代号填)。
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体。
上述反应的离子方程式如下,请将方程式补写完整_______ 。
___________ +_______H2O=_______Fe(OH)3(胶体)+________O2↑+_________OH-
+_______H2O=_______Fe(OH)3(胶体)+________O2↑+_________OH-
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①写出FeCl3溶液与金属铜发生反应的化学方程式___________ 。
②某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,采用下列步骤:

请写出上述过程中滤渣③中所含成分的化学式_________ ,物质⑥的化学式___________ 。
(4)把1.1g铁、铝混合物溶于200ml5mol/L盐酸中,反应后盐酸的浓度变为4.6mol/L(溶液体积变化忽略不计)。求①反应中消耗HCl的物质的量________________ 。
②该混合物中铝的物质的量________________ ,铁的物质的量 _________ 。
(1)下列铁的化合物中,可以由单质直接化合得到的是___________(用字母代号填)。
| A.Fe(OH)2 | B.FeCl3 | C.Fe(OH)3 | D.Fe3O4 |
上述反应的离子方程式如下,请将方程式补写完整
___________
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①写出FeCl3溶液与金属铜发生反应的化学方程式
②某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,采用下列步骤:

请写出上述过程中滤渣③中所含成分的化学式
(4)把1.1g铁、铝混合物溶于200ml5mol/L盐酸中,反应后盐酸的浓度变为4.6mol/L(溶液体积变化忽略不计)。求①反应中消耗HCl的物质的量
②该混合物中铝的物质的量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


