解答题-原理综合题 适中0.65 引用2 组卷426
化学反应是有历程的。研究反应机理对于认识反应和调控反应意义重大。
I:NO和H2可以反应生成N2和水蒸气,其中每生成7gN2,放出166kJ的热量。该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),其反应历程包含下列两步:
①2NO+H2=N2+H2O2(慢) Ea1
②H2O2+H2=2H2O(快) Ea2
T℃时测得有关实验数据如下:
(1)该反应的热化学方程式为___________ 。
(2)活化能Ea1___________ Ea2(填“>或<或=”)。
(3)m=___________ ,n=___________ 。
II:催化剂参与反应过程,能加快反应速率。
(4)2SO2+O2=2SO3的速率很慢,NO和NO2都可以作为该反应的催化剂,发生两步基元反应,快速生成SO3。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式___________ 。
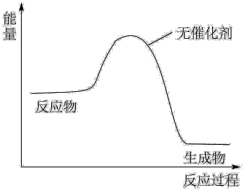
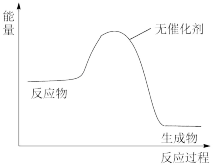
(5)请在下图中画出加入催化剂时的能量变化过程__________ (已知该两步反应均为放热反应)。
I:NO和H2可以反应生成N2和水蒸气,其中每生成7gN2,放出166kJ的热量。该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),其反应历程包含下列两步:
①2NO+H2=N2+H2O2(慢) Ea1
②H2O2+H2=2H2O(快) Ea2
T℃时测得有关实验数据如下:
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| I | 0.0060 | 0.0010 | 1.8×10-4 |
| II | 0.0060 | 0.0020 | 3.6×10-4 |
| III | 0.0010 | 0.0060 | 3.0×10-5 |
| IV | 0.0020 | 0.0060 | 1.2×10-4 |
(1)该反应的热化学方程式为
(2)活化能Ea1
(3)m=
II:催化剂参与反应过程,能加快反应速率。
(4)2SO2+O2=2SO3的速率很慢,NO和NO2都可以作为该反应的催化剂,发生两步基元反应,快速生成SO3。请结合催化剂的特点,写出NO做催化剂时,这两步基元反应的方程式
(5)请在下图中画出加入催化剂时的能量变化过程

20-21高一下·北京海淀·期末
类题推荐
反应2NO(g)+2H2(g)=N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),其反应包含下列两步:①2NO+H2=N2+H2O2(慢)②H2O2+H2=2H2O(快)
T℃时测得有关实验数据如下:
下列说法错误的是
T℃时测得有关实验数据如下:
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
| A.整个反应速率由第①步反应决定 |
| B.正反应的活化能一定是①<② |
| C.该反应速率表达式:v=5000c2(NO)·c(H2) |
| D.该反应的热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g)ΔH=-664kJ·mol-1 |
反应2NO(g)+2H2(g)=N2(g)+2H2O(g)中,每生成7 g N2放出166 kJ的热量,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),该反应包含下列两步:①2NO+H2=N2+H2O2(慢),②H2O2+H2=2H2O(快)。T ℃时测得有关实验数据如表:
下列说法错误的是
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| Ⅰ | 0.006 0 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.006 0 | 0.002 0 | 3.6×10-4 |
| Ⅲ | 0.001 0 | 0.006 0 | 3.0×10-5 |
| Ⅳ | 0.002 0 | 0.006 0 | 1.2×10-4 |
| A.整个反应速度由第①步反应决定 |
| B.该反应速率表达式:v=5000c2(NO)·c(H2) |
| C.正反应的活化能:①>② |
| D.该反应的热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g) ΔH=-332 kJ·mol-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网