多选题 适中0.65 引用5 组卷631
在恒温条件下,向盛有足量NaCl(s)的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) ΔH1<0 K1
NaNO3(s)+ClNO(g) ΔH1<0 K1
②2NO(g)+Cl2(g) 2ClNO(g) ΔH2<0 K2
2ClNO(g) ΔH2<0 K2
10分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
①2NO2(g)+NaCl(s)
②2NO(g)+Cl2(g)
10分钟时反应达到平衡,测得体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol·L-1·min-1。下列说法正确的是
| A.平衡后c(NO)=2.5×10-2mol·L-1 |
| B.平衡时NO的转化率为50% |
| C.其它条件保持不变,反应在绝热条件下进行,则平衡常数K2增大 |
| D.反应4NO2(g)+2NaCl(s) |
2021·山东德州·二模
类题推荐
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH。在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)= 0.1mol,NO2的转化率为α。下列叙述中正确的是| A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1 |
| B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C.若升高温度,平衡逆向移动,则该反应的ΔH>0 |
| D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
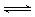 2ClNO(g)
2ClNO(g)

