多选题 较易0.85 引用1 组卷166
对于Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)ΔH<0kJ·mol-1的化学反应,下列说法一定正确的是
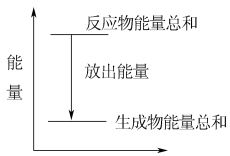

| A.反应前后能量关系可用如图所示 |
| B.1mol锌所含的能量高于1molH2所含的能量 |
| C.若将该反应设计成原电池,锌为负极 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
20-21高一下·江苏苏州·阶段练习
类题推荐
对于Zn(s) + H2SO4(aq) ═ ZnSO4(aq) + H2(g) △H=?的化学反应,下列叙述不正确的是
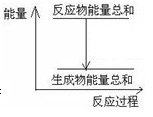

| A.反应过程中能量关系如图所示,则该反应为放热反应 |
| B.化学反应的反应热与反应方程式的计量数有关 |
| C.若将该反应设计成原电池,锌为负极 |
| D.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g) ΔH<0的化学反应下列叙述不正确的是
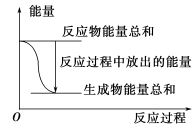

| A.反应过程中能量关系可用上图表示 |
| B.ΔH的值与反应方程式的计量系数有关 |
| C.若将该反应设计成原电池,锌为负极 |
| D.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是
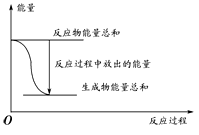
| A.反应过程中能量关系如上图表示,则该反应为放热反应 |
| B.若将该反应设计成原电池,锌为负极 |
| C.化学反应的焓变与反应方程式的计量数有关 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


