解答题-原理综合题 适中0.65 引用1 组卷130
资源化利用碳及其化合物具有重要意义。
(1)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
Ⅰ.

Ⅱ.

反应Ⅱ中,正反应的活化能_______ (填“ ”、“
”、“ ”或“
”或“ ”)逆反应的活化能。
”)逆反应的活化能。
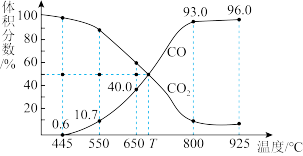
(2)在一定温度下,向某体积可变的恒压( )密闭容器中加入
)密闭容器中加入 与足量的碳发生反应
与足量的碳发生反应 ,平衡时体系中气体体积分数与温度关系如图2所示。
,平衡时体系中气体体积分数与温度关系如图2所示。
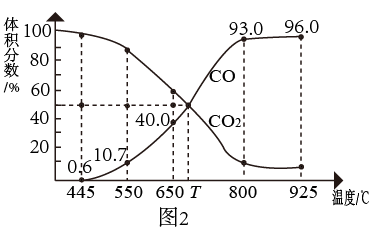
①650℃时,反应达平衡后 的转化率为
的转化率为_______ ;
②T℃时,在 恒容密闭容器中加入
恒容密闭容器中加入 与足量的碳,
与足量的碳, 后测得
后测得 为
为 (标况下),则
(标况下),则
_______ ;上述反应达到平衡状态时,下列说法正确的是_______ (填序号);
a.单位时间内生成的CO2的物质的量是CO的两倍
b.容器中气体的压强不随时间而变化
c.升高温度,再次达到平衡时,C的质量减少
d.保持其它条件不变,充入惰性气体,反应速率减小,平衡移动
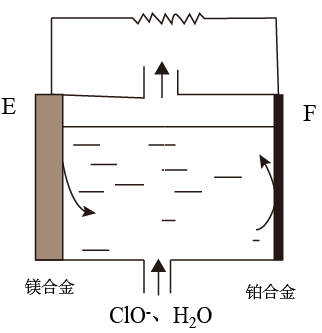
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。如图为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的_______ (填“正”或“负”)极。F电极上的电极反应式为_______ 。
(1)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
Ⅰ.
Ⅱ.
反应Ⅱ中,正反应的活化能
(2)在一定温度下,向某体积可变的恒压(

①650℃时,反应达平衡后
②T℃时,在
a.单位时间内生成的CO2的物质的量是CO的两倍
b.容器中气体的压强不随时间而变化
c.升高温度,再次达到平衡时,C的质量减少
d.保持其它条件不变,充入惰性气体,反应速率减小,平衡移动
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。如图为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的

21-22高三上·广东梅州·阶段练习
类题推荐
资源化利用CO具有重要意义。
(1)CO可设计成燃料电池,熔融Li2CO3和Na2CO3的混合物作为燃料电池的电解质,氧化剂是含CO2的O2,工作时正极反应为__________________ ,以该燃料电池为电源处理含氮氧化物废气,可回收硝酸,同时制得副产物氢气,装置如图所示(电极均为石墨电极)。该装置中应选用_______ (填“阴”或“阳”)离子交换膜,写出电解时NO2发生反应的电极反应式:___________________ 。

(2)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
试计算,试计算,X=_________ 。
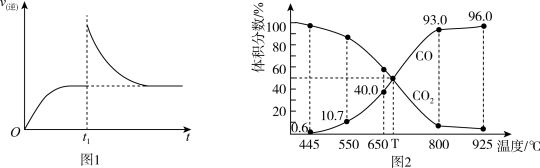
T1℃时,向某恒温密闭容器中加入一定量的Fe2O3和C,发生反应I,反应达到平衡后,在t1时刻改变某条件,v(逆)随时间(t)的变化关系如图所示,则t1时刻改变的条件可能是_____________________ 。
a.保持温度、体积不变,使用催化剂 b.保持体积不变,升高温度
c.保持温度不变,压缩容器体积 d.保持温度、体积不变,充入CO
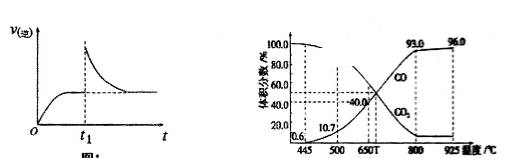
(3)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1mol CO2与足量的碳发生反应III,平衡时体系中气体体积分数与温度的关系如图所示。
①650℃时,反应达平衡后CO2的转化率为____________ 。
②T℃时,该反应达到平衡时下列说法不正确的是__________________ 。
a.气体密度保持不变
b.2v正(CO2)=v正(CO)
c.若保持其它条件不变再充入等体积的CO2和CO,平衡向逆反应方向移动
d.若保持其它条件不变再充入惰性气体,v正、v逆均减小,平衡不移动
e.若其它条件不变将容器体积压缩至一半并维持体积不变,再次达平衡时压强小于原平衡的2倍
③根据图中数据,计算反应III在T℃时用平衡分压代替平衡浓度表示的化学平衡常数KP=___________ (设总压强为P总,用含P总的代数式表示)
(1)CO可设计成燃料电池,熔融Li2CO3和Na2CO3的混合物作为燃料电池的电解质,氧化剂是含CO2的O2,工作时正极反应为

(2)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
| 反应 | △H(kJ/mol) |
I. Fe2O3(s)+3C(s)  2Fe(s)+3CO(g) 2Fe(s)+3CO(g) | +489 |
II. Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) 2Fe(s)+3CO2(g) | -27 |
III. C(s)+CO2(g)  2CO(g) 2CO(g) | X |
试计算,试计算,X=
T1℃时,向某恒温密闭容器中加入一定量的Fe2O3和C,发生反应I,反应达到平衡后,在t1时刻改变某条件,v(逆)随时间(t)的变化关系如图所示,则t1时刻改变的条件可能是
a.保持温度、体积不变,使用催化剂 b.保持体积不变,升高温度
c.保持温度不变,压缩容器体积 d.保持温度、体积不变,充入CO

(3)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1mol CO2与足量的碳发生反应III,平衡时体系中气体体积分数与温度的关系如图所示。
①650℃时,反应达平衡后CO2的转化率为
②T℃时,该反应达到平衡时下列说法不正确的是
a.气体密度保持不变
b.2v正(CO2)=v正(CO)
c.若保持其它条件不变再充入等体积的CO2和CO,平衡向逆反应方向移动
d.若保持其它条件不变再充入惰性气体,v正、v逆均减小,平衡不移动
e.若其它条件不变将容器体积压缩至一半并维持体积不变,再次达平衡时压强小于原平衡的2倍
③根据图中数据,计算反应III在T℃时用平衡分压代替平衡浓度表示的化学平衡常数KP=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网