解答题-无机推断题 适中0.65 引用1 组卷135
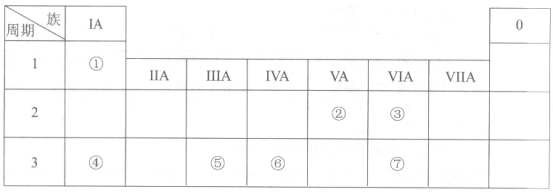
如表列出了①~⑦七种元素在周期表中的位置。请按要求回答:
(1)七种元素中,原子半径最大的是(填元素符号)___________ 。
(2)③与⑦的简单氢化物中,稳定性较强的是(填化学式)___________ ,该物质的分子为___________ (填“极性”或“非极性”)分子。
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为___________ 。
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为___________ 。
(5)由①、②、③三种元素组成的离子化合物是___________ ,检验该化合物中阳离子的方法是___________ 。
(6)下列事实能说明O的非金属性比S的非金属性强的是___________(填字母代号)。
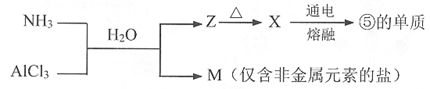
(7)含有上述元素的物质间存在如图转化。
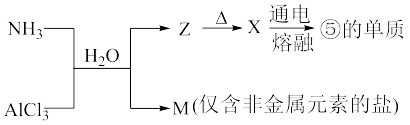
M所含的化学键类型是___________ ,实验室检验AlCl3是否为离子化合物的方法___________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)七种元素中,原子半径最大的是(填元素符号)
(2)③与⑦的简单氢化物中,稳定性较强的是(填化学式)
(3)元素②形成的一种氢化物常用作火箭燃料,则该物质的电子式为
(4)元素④的最高价氧化物对应的水化物与元素⑤的最高价氧化物对应的水化物发生反应的离子方程式为
(5)由①、②、③三种元素组成的离子化合物是
(6)下列事实能说明O的非金属性比S的非金属性强的是___________(填字母代号)。
| A.O2与H2S溶液反应,溶液变浑浊 |
| B.加热条件下H2S比H2O更容易分解 |
| C.在氧化还原反应中,1 mol O2比1 mol S得电子多 |
| D.H2O的沸点比H2S高 |
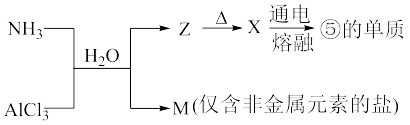
M所含的化学键类型是
21-22高三上·黑龙江哈尔滨·开学考试
类题推荐
如表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素③的原子结构示意图是___________ ,以上元素的最高价氧化物形成的水化物酸性最强的是___________ (填分子式)。
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为___________ (用离子符号表示);②、③两种元素的最高价氧化物对应的水化物碱性由弱到强的顺序是___________ (用化学式表示)。
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为___________ 。
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式___________ 。
(5)设计一个实验比较②与③的金属性强弱___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ⑦ | ||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
请按要求回答下列问题:
(1)元素③的原子结构示意图是
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式
(5)设计一个实验比较②与③的金属性强弱
如表为元素周期表的一部分,请参照元素在表中①-⑩的位置,用相应的化学用语回答下列问题:
(1)形成化合物种类最多的元素在周期表中的位置是_______ 。
(2)元素⑦的简单离子结构示意图为______ 。
(3)元素④、⑤、⑨形成的简单氢化物稳定性由弱到强的顺序为______ (用化学式作答,下同)。元素③、⑧、⑩形成的最高价氧化物对应的水化物的酸性由强到弱的顺序为______ 。
(4)10种元素中,金属性最强的是______ (填序号),该元素与④形成的含有非极性共价键的化合物的电子式为______ 。
(5)元素②的单质和元素⑨的最高价氧化物对应的水化物反应的化学方程式为______ 。某同学为检验气体产物设计了如图的实验装置,据此回答问题:
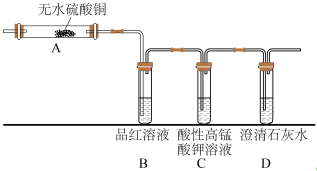
①B中的实验现象是______ ,证明产物中有______ 。
②装置C的作用是______ ,发生的化学反应方程式为______ 。
(6)下列事实能说明⑩元素原子得电子能力比⑨元素原子强的是______ (填序号)。
①氢化物的溶解度:⑩>⑨
②氢化物的酸性:⑩>⑨
③氢化物的稳定性:⑩>⑨
④氢化物的还原性:⑩<⑨
⑤最高价氧化物对应的水化物的酸性:⑩>⑨
⑥单质的氧化性:⑩>⑨
⑦对应阴离子的还原性:⑩<⑨
⑧单质⑩通入⑨的氢化物水溶液中可生成单质⑨
⑨在周期表中⑩处于⑨同周期的右侧
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)元素⑦的简单离子结构示意图为
(3)元素④、⑤、⑨形成的简单氢化物稳定性由弱到强的顺序为
(4)10种元素中,金属性最强的是
(5)元素②的单质和元素⑨的最高价氧化物对应的水化物反应的化学方程式为

①B中的实验现象是
②装置C的作用是
(6)下列事实能说明⑩元素原子得电子能力比⑨元素原子强的是
①氢化物的溶解度:⑩>⑨
②氢化物的酸性:⑩>⑨
③氢化物的稳定性:⑩>⑨
④氢化物的还原性:⑩<⑨
⑤最高价氧化物对应的水化物的酸性:⑩>⑨
⑥单质的氧化性:⑩>⑨
⑦对应阴离子的还原性:⑩<⑨
⑧单质⑩通入⑨的氢化物水溶液中可生成单质⑨
⑨在周期表中⑩处于⑨同周期的右侧
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网