解答题-工业流程题 较易0.85 引用1 组卷99
实验室以含有Ca2+、Mg2+、Brˉ、Clˉ等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
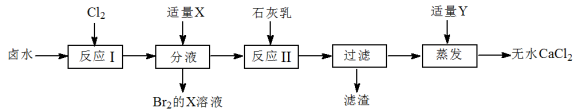
(1)试剂X可以选择___________(填字母序号)。
(2)试剂Y可以选择 ___________(填字母序号)
(3)反应Ⅰ的离子反应方程式是___________ 。
(4)分液所用主要仪器的名称是___________ 。
(5)已知:反应Ⅱ加石灰乳,调节溶液的pH范围是___________ 。其目的是___________ 。

(1)试剂X可以选择___________(填字母序号)。
| A.酒精 | B.四氯化碳 | C.水 | D.苯 |
| A.稀盐酸 | B.稀硫酸 | C.氢氧化钠 | D.氯化钠 |
(4)分液所用主要仪器的名称是
| 开始沉淀的pH | 完全沉淀的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OHˉ)=1.8mol/L |
(5)已知:反应Ⅱ加石灰乳,调节溶液的pH范围是
21-22高二上·内蒙古赤峰·开学考试
类题推荐
以含有Ca2+、Mg2+、Clˉ、SO42ˉ、Brˉ 等离子的卤水为主要原料可制备金属镁和溴。流程如下:
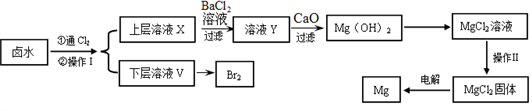
(1)操作Ⅰ的名称是______ ,所用主要玻璃仪器的名称是_________ 、_________ ;需要选择的试剂是____________ (填序号)。
(2)通氯气反应的离子方程式__________________________________ 。
(3)证明SO42ˉ完全沉淀的方法是______________________________ 。
(4)CaO用来调节溶液Y的pH,可以使Mg2+沉淀完全,由下表中数据可知,理论上应控制pH范围是__________ 。
(5)操作Ⅱ用下图所示操作______________ 实现(填“能”或“不能”)。原因是______________________________ (用化学方程式解释)。
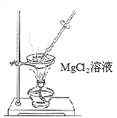
(6)工业上用惰性电极电解熔融状态下的氯化镁来冶炼镁,不能直接电解氯化镁溶液的原因是___________________________ (用离子方程式表示)。
(7)在探究Mg(OH)2溶解性的实验中,发现向装有少量Mg(OH)2浊液的试管中加入适量NH4Cl晶体,充分振荡后浊液会变澄清,请用化学平衡的原理解释浊液变澄清的原因_________________________________ 。

(1)操作Ⅰ的名称是
a.乙醇 b.苯 c.四氯化碳 d.裂化汽油
(2)通氯气反应的离子方程式
(3)证明SO42ˉ完全沉淀的方法是
(4)CaO用来调节溶液Y的pH,可以使Mg2+沉淀完全,由下表中数据可知,理论上应控制pH范围是
开始沉淀时 | 沉淀完全时 | |
Mg2+ | pH=9.6 | pH=11.0 |
Ca2+ | pH=12.2 | c(OH-) =1.8mol/L |

(6)工业上用惰性电极电解熔融状态下的氯化镁来冶炼镁,不能直接电解氯化镁溶液的原因是
(7)在探究Mg(OH)2溶解性的实验中,发现向装有少量Mg(OH)2浊液的试管中加入适量NH4Cl晶体,充分振荡后浊液会变澄清,请用化学平衡的原理解释浊液变澄清的原因
某科研人员以废镍催化剂(主要成分为 ,另含
,另含 )为原料回收镍,工艺流程如图。
)为原料回收镍,工艺流程如图。
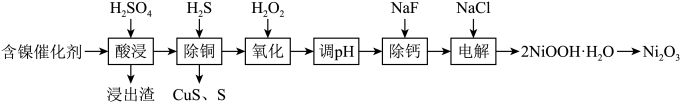
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表。
如表。
回答下列问题:
(1)浸出渣主要成分为_______ 、______ (填化学式) ,酸浸时除去不溶性杂质的操作名称是______ 。
(2)“除铜”时, 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(3)加入H2O2的目的是将溶液中 氧化为
氧化为 ,温度需控制在
,温度需控制在 之间,在“氧化”时温度不能太高的原因是
之间,在“氧化”时温度不能太高的原因是______ 。
(4)“调 ” 是为了除去
” 是为了除去 ,操作时需控制pH值的范围为
,操作时需控制pH值的范围为____ ,此时试剂可以选择____ (填字母序号)。
A.Ni(OH)2 B.Na2O C.氨水 D.NiCO3
(5)“除钙”后,若溶液中 浓度为
浓度为 ,c(Ca2+)=
,c(Ca2+)=____ mol·L-1。[常温时Ksp(CaF2)=2.7×10-11]

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的
| 氢氧化物 | |||
| 开始沉淀的 | 1.5 | 6.5 | 8.2 |
| 沉淀完全的 | 3.7 | 9.7 | 9.2 |
(1)浸出渣主要成分为
(2)“除铜”时,
(3)加入H2O2的目的是将溶液中
(4)“调
A.Ni(OH)2 B.Na2O C.氨水 D.NiCO3
(5)“除钙”后,若溶液中
硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO。 某探究性学习小组的同学设计以下实验方案,将硫酸渣中金属元素分别转化为氢氧化物沉淀而分离开来。
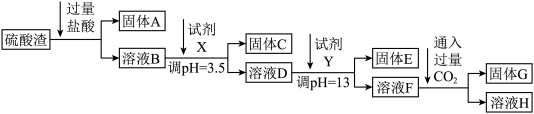
已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)工业上用固体A作原料制取水玻璃的化学方程式为_______ 。
(2)固体E的化学式为_______ 。
(3)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要_______ 。
(4)上述流程中的试剂Y最好选用下列中的_______ (选填字母编号)。
A.水 B.硫酸 C.氨水 D.氢氧化钠
(5)写出反应F→H的离子方程式_______ 。

已知常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时pH | 1.9 | 3.7 | 9.6 |
| 完全沉淀时pH | 3.2 | 5.2 | 11.0 |
(2)固体E的化学式为
(3)实验室用11.9mol/L的浓盐酸配制250mL3.0mol/L的稀盐酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要
(4)上述流程中的试剂Y最好选用下列中的
A.水 B.硫酸 C.氨水 D.氢氧化钠
(5)写出反应F→H的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


