解答题-工业流程题 适中0.65 引用1 组卷138
硼酸(H3BO3)是一种重要的化工原料。工业上以硼镁矿(主要成分为Mg2B2O5·H2O和SiO2,还含有少量的Fe3O4、Al2O3等杂质)为原料生产硼酸和MgCl2·6H2O,其工艺流程如图:
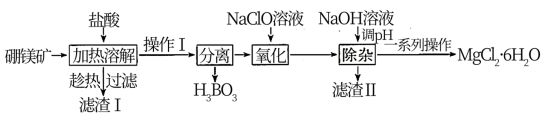
已知:H3BO3能溶于水,且其溶解度随温度的升高而升高。回答下列问题:
(1)为加快“加热溶解”的速率,可采取的措施是___ (请写出两条),“加热溶解”时主要反应的化学方程式为___ 。
(2)滤渣Ⅰ和滤渣Ⅱ的主要成分分别为____ 、____ (填化学式)。
(3)“趁热过滤”的目的是___ ,操作Ⅰ为____ 。
(4)“氧化”时反应的离子方程式为____ 。
(5)室温下,“除杂”时调节pH=5,则此时溶液中c(Fe3+)=____ mol·L-1。已知:室温下Ksp[Fe(OH)3]=2.8×10-39。

已知:H3BO3能溶于水,且其溶解度随温度的升高而升高。回答下列问题:
(1)为加快“加热溶解”的速率,可采取的措施是
(2)滤渣Ⅰ和滤渣Ⅱ的主要成分分别为
(3)“趁热过滤”的目的是
(4)“氧化”时反应的离子方程式为
(5)室温下,“除杂”时调节pH=5,则此时溶液中c(Fe3+)=
21-22高三上·河北邯郸·开学考试
类题推荐
I.工业上制取纯净的CuCl2•2H2O的主要过程是:①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;②对①所得滤液按下列步骤进行操作:
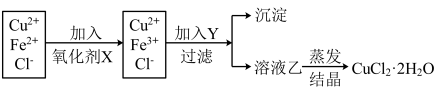
已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答下列问题:
(1)加Y的目的是_____ ,生产中Y可选用:______ 。
(2)蒸发结晶时,直接在空气中加热蒸干溶液乙得不到CuCl2•2H2O晶体,可以采用减压低温蒸发结晶的方法,在蒸发过程中需不断通入_____ 气体,且不能蒸干。
II.以红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2等)为原料制备Ni(OH)2的工艺流程如图:
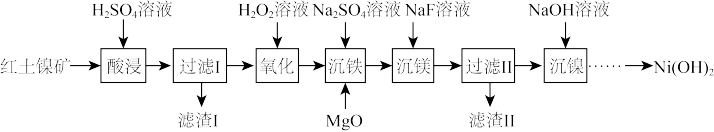
(3)“酸浸”时,加快化学反应速率的措施_____ (写一条即可)。滤渣1的成分为_____ (填化学式)。
(4)“氧化”时,Fe2+发生反应的离子方程式为_____ 。
(5)MgO的作用是调节溶液pH使Fe3+沉淀,根据表中的数据,则调节溶液pH的范围是_____ 。
(6)室温时,若“沉镍”后的滤液c(Ni2+)<1×10-5mol•L-1,则滤液中pH>_____ 。(Ksp[Ni(OH)2]=1×10-15)

已知Cu2+、Fe2+在pH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答下列问题:
(1)加Y的目的是
(2)蒸发结晶时,直接在空气中加热蒸干溶液乙得不到CuCl2•2H2O晶体,可以采用减压低温蒸发结晶的方法,在蒸发过程中需不断通入
II.以红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2等)为原料制备Ni(OH)2的工艺流程如图:

(3)“酸浸”时,加快化学反应速率的措施
(4)“氧化”时,Fe2+发生反应的离子方程式为
(5)MgO的作用是调节溶液pH使Fe3+沉淀,根据表中的数据,则调节溶液pH的范围是
| 金属离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ |
| 开始沉淀的pH | 6.3 | 1.5 | 8.9 | 6.9 |
| 沉淀完全的pH | 8.3 | 2.8 | 10.9 | 8.9 |
(6)室温时,若“沉镍”后的滤液c(Ni2+)<1×10-5mol•L-1,则滤液中pH>
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网