填空题 较易0.85 引用1 组卷278
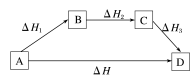
根据如下两个反应,选用上述两种方法,计算出C(s)+ O2(g)=CO(g)的反应热ΔH。
O2(g)=CO(g)的反应热ΔH。
I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+ O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
①“虚拟路径”法
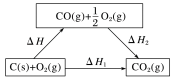
反应C(s)+O2(g)=CO2(g)的途径可设计如下:
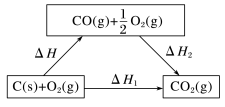
则ΔH=_______ =_______ kJ·mol-1。
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=___ =___ kJ·mol-1。
I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+
①“虚拟路径”法
反应C(s)+O2(g)=CO2(g)的途径可设计如下:

则ΔH=
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=
20-21高二·全国·课前预习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网