解答题-实验探究题 适中0.65 引用4 组卷191
某化学兴趣小组进行锌与硫酸溶液反应的实验,并用大气球收集产生的气体。同学们在收集过程中闻到一股刺激性气味,同时发现充满气体的气球在空气中有些下沉,有些悬浮,还有些上浮。大家对这些现象很感兴趣,进行了相关探究活动。
【查阅资料】
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气体和水。
(2)SO2有刺激性气味,易溶于水,能使品红溶液褪色。SO2和CO2化学性质相似,都能和NaOH等碱溶液反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的平均相对分子质量为29。
【提出猜想】
猜想一:气球内的气体为SO2;
猜想二:气球内的气体为SO2和H2;
猜想三:气球内的气体为H2。
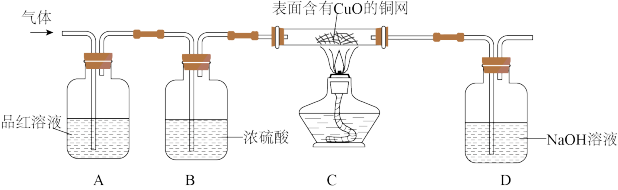
【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同气球内的气体进行探究。
(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是___ 。
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是___ 。
(3)乙同学观察到___ ,说明猜想二正确。
(4)丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
【实验结论】通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
【拓展反思】
(4)下列物质中不能由金属和稀硫酸反应直接得到的是___ 。
(5)浓硫酸与铜在加热的条件下反应生成硫酸铜、二氧化硫气体和水,而稀硫酸与铜即使加热也不能反应。这说明:某溶液的化学性质除了与溶质的性质有关外,还可能与下列中的有关___ (填序号)。
(6)锌与铜分别和浓硫酸在一定条件下都可以反应产生二氧化硫,若选择铜与浓硫酸在加热的条件下反应制取二氧化硫气体,其优点是___ 。
(7)实验中下沉的气球内一定含有的气体是___ 。(填化学式)
【查阅资料】
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气体和水。
(2)SO2有刺激性气味,易溶于水,能使品红溶液褪色。SO2和CO2化学性质相似,都能和NaOH等碱溶液反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的平均相对分子质量为29。
【提出猜想】
猜想一:气球内的气体为SO2;
猜想二:气球内的气体为SO2和H2;
猜想三:气球内的气体为H2。
【实验探究】针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同气球内的气体进行探究。
(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是
(3)乙同学观察到
(4)丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
【实验结论】通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
【拓展反思】
(4)下列物质中不能由金属和稀硫酸反应直接得到的是
| A.Al2(SO4)3 | B.Fe2(SO4)3 | C.MgSO4 | D.ZnSO4 |
| A.溶质的质量分数 | B.溶液的质量 |
| C.溶液的体积 | D.溶质的相对分子质量 |
(7)实验中下沉的气球内一定含有的气体是
21-22高一上·四川雅安·开学考试
类题推荐
I.实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。
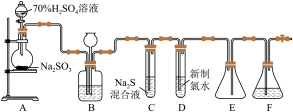
(1)盛装70% H2SO4溶液的仪器名称为___________ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为___________ 。
(5)装置E的作用是___________ 。装置F中为___________ 溶液。
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
说明在严格控制用量的情况下,二氧化硫可被添加到食品中作为漂白剂、防腐剂和___________ (填“氧化剂”或“抗氧化剂”)。
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:
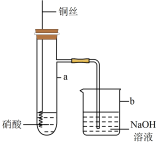
(7)组装好装置后进行实验之前需先进行___________ 。
(8)写出实验Ⅰ中产生的无色气体化学式___________ 。
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式___________ 。
(10)装置中采用可拉动铜丝的优点是___________ (写一点)。
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。

(1)盛装70% H2SO4溶液的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
(6)二氧化硫可作为食品添加剂。
查阅资料:国家食品添加剂使用标准中二氧化硫最大使用量如下表
| 食品名称 | 食糖 | 葡萄酒 | 水果干类 |
| SO2最大使用量 | 0.1g•kg-1 | 0.25g•kg-1 | 1g•kg-1 |
II.利用下图所示装置进行铜与硝酸反应的实验,得到的实验现象如下表:

| 序号 | 实验试剂(20℃) | 实验现象 |
| Ⅰ | 铜丝、2mL稀硝酸 | 铜丝逐渐变细,有气泡产生,a中先产生无色气体后略有红棕色,溶液变蓝 |
| Ⅱ | 铜丝、2mL浓硝酸 | 反应剧烈,铜丝逐渐变细,a中上方出现红棕色气体,溶液变绿 |
(8)写出实验Ⅰ中产生的无色气体化学式
(9)写出实验Ⅱ中铜与浓硝酸反应的离子方程式
(10)装置中采用可拉动铜丝的优点是
(11)针对Ⅰ中溶液呈蓝色,Ⅱ中溶液呈绿色。甲同学推测溶液的颜色与硝酸铜的质量分数有关,而乙同学推测Ⅱ中溶液呈绿色的原因是NO2在硝酸铜溶液中达到饱和所致。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是___________。
| A.加热绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
某兴趣小组为拓展对SO2还原性和氧化性的认识,进行了下列两组探究实验。
I.探究SO2和 Fe(NO3)3溶液反应,反应装置如图所示:
②该实验条件下不考虑Cl-被酸性KMnO4溶液氧化。
回答下列问题:
(1)盛装浓硫酸的仪器名称为__________ 。
(2)A中发生的反应的化学反应式为__________ 。
Ⅱ.如图进行实验,装置B中产生了白色沉淀,经检验,其成分为BaSO4。分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+反应;
猜想2:在酸性条件下SO2与 反应;
反应;
猜想3:……
(3)甲同学从装置B中取出少量反应后的溶液,该溶液能使KMnO4溶液褪色。甲据此认为猜想1成立。乙同学认为该实验不严谨,理由是________________ 。
(4)请你设计实验验证猜想2,并完成表中内容(提示: 在不同条件下的还原产物较复杂,有时难以观察到气体产生。除了上述实验提供的试剂外,可供选择的药品有:NaNO3固体和盐酸等。)
在不同条件下的还原产物较复杂,有时难以观察到气体产生。除了上述实验提供的试剂外,可供选择的药品有:NaNO3固体和盐酸等。)
①完善表格:pH=_____ ,c( )为
)为______ mol·L-1。
②尾气处理装置应选择______ (填序号)。
查阅资料: 水溶液显棕色,
水溶液显棕色,
 CuCl(白色)+2Cl-
CuCl(白色)+2Cl-
(5)通过上述两组对比实验,SO2与铜反应的条件是______________ 。
(6)配平SO2在盐酸中和铜反应的离子方程式______ 。
_____Cu+_____SO2+______H++______Cl-=_______CuS+_______ +______H2O
+______H2O
I.探究SO2和 Fe(NO3)3溶液反应,反应装置如图所示:
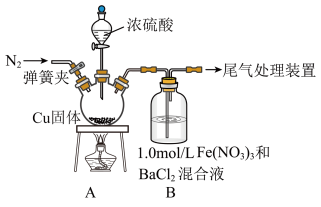
②该实验条件下不考虑Cl-被酸性KMnO4溶液氧化。
回答下列问题:
(1)盛装浓硫酸的仪器名称为
(2)A中发生的反应的化学反应式为
Ⅱ.如图进行实验,装置B中产生了白色沉淀,经检验,其成分为BaSO4。分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+反应;
猜想2:在酸性条件下SO2与
猜想3:……
(3)甲同学从装置B中取出少量反应后的溶液,该溶液能使KMnO4溶液褪色。甲据此认为猜想1成立。乙同学认为该实验不严谨,理由是
(4)请你设计实验验证猜想2,并完成表中内容(提示:
| 实验步骤 | 预期现象和结论 |
| a.配溶液,用NaNO3和盐酸配成pH=_______,c( | 若装置B中有白色沉淀生成,猜想2成立。 |
| b.打开弹簧夹,向装置中通入一段时间的N2,关闭弹簧夹。打开分液漏斗活塞,向三颈烧瓶中滴加浓硫酸并加热。 | 若装置B中无白色沉淀生成,猜想2不成立。 |
②尾气处理装置应选择

| 实验① | 实验② |
|
|
(5)通过上述两组对比实验,SO2与铜反应的条件是
(6)配平SO2在盐酸中和铜反应的离子方程式
_____Cu+_____SO2+______H++______Cl-=_______CuS+_______
Li2S(硫化锂)是一种潜在的锂电池的电解质材料。某小组选择下列装置(装置B使用两次)利用氢气还原硫酸锂制备硫化锂,原理是Li2SO4+4H2 Li2S+4H2O。已知:Li2S易潮解,在加热条件下易被空气中的O2氧化。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备H2。
Li2S+4H2O。已知:Li2S易潮解,在加热条件下易被空气中的O2氧化。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备H2。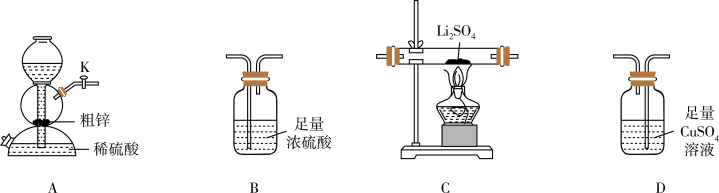
请回答下列问题:
(1)按气流从左至右,装置的连接顺序是A→____ (填字母)。
(2)其他条件相同,粗锌与稀硫酸反应比纯锌____ (填“快”或“慢”)。实验中观察到装置D中产生黑色沉淀,其离子方程式为____ 。
(3)还可利用装置A制备的下列气体是____ (填字母)。
A.SO2:70%硫酸、亚硫酸钠粉末
B.CO2:稀盐酸、大理石
C.Cl2:浓盐酸、二氧化锰
(4)实验完毕后,采用图1、图2(夹持装置已略去)装置对装置A中混合物进行分离可得到副产物皓矾(ZnSO4·7H2O)晶体。先选择图1装置进行过滤,并将滤液进行蒸发浓缩、降温结晶,再选择图2装置过滤,得到粗皓矾晶体。
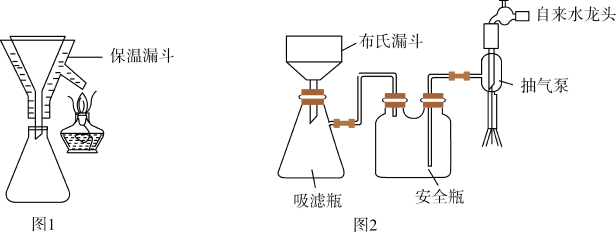
下列有关说法正确的是____ (填字母)。
(5)欲探究Li2S产品的成分,现进行如表实验:
①由上述实验II可知,Li2S样品中含有____ 杂质(填化学式),产生该杂质的原因可能是____ 。
②测定产品纯度的方法:取wgLi2S样品加入V1mLc1mol·L-1稀硫酸(过量)中,充分反应后,煮沸溶液以除去残留的酸性气体;滴加酚酞溶液作指示剂,用c2mol·L-1标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液V2mL。若该Li2S样品中杂质不参加反应,用上述方法测得的Li2S样品的纯度为____ %(用含V1、V2、c1、c2、w的代数式表示)。

请回答下列问题:
(1)按气流从左至右,装置的连接顺序是A→
(2)其他条件相同,粗锌与稀硫酸反应比纯锌
(3)还可利用装置A制备的下列气体是
A.SO2:70%硫酸、亚硫酸钠粉末
B.CO2:稀盐酸、大理石
C.Cl2:浓盐酸、二氧化锰
(4)实验完毕后,采用图1、图2(夹持装置已略去)装置对装置A中混合物进行分离可得到副产物皓矾(ZnSO4·7H2O)晶体。先选择图1装置进行过滤,并将滤液进行蒸发浓缩、降温结晶,再选择图2装置过滤,得到粗皓矾晶体。

下列有关说法正确的是
| A.采用图1装置过滤的优点是避免析出ZnSO4·7H2O |
| B.采用图1装置过滤主要是分离FeSO4·7H2O和ZnSO4溶液 |
| C.粗皓矾晶体中可能含少量CuSO4·5H2O杂质 |
| D.采用图2装置过滤的优点是过滤速度快 |
| 实验 | 操作与现象 | 结论 |
| I | 取少量Li2S样品,滴加足量的稀盐酸,将气体通入品红溶液中,溶液褪色 | 样品含Li2SO3 |
| II | 在实验I的溶液中滴加BaCl2溶液,产生白色沉淀 | 样品含 |
②测定产品纯度的方法:取wgLi2S样品加入V1mLc1mol·L-1稀硫酸(过量)中,充分反应后,煮沸溶液以除去残留的酸性气体;滴加酚酞溶液作指示剂,用c2mol·L-1标准NaOH溶液滴定过量的硫酸,消耗NaOH溶液V2mL。若该Li2S样品中杂质不参加反应,用上述方法测得的Li2S样品的纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




