解答题-工业流程题 较难0.4 引用1 组卷102
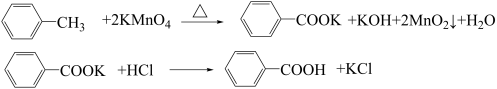
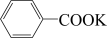
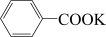
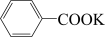
苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
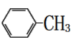 +2KMnO4
+2KMnO4
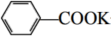 +2MnO2↓+H2O
+2MnO2↓+H2O
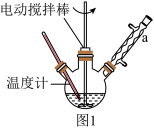
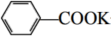 +HCl
+HCl
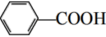 +KCl
+KCl
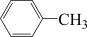
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
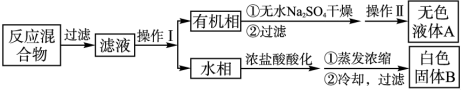
已知:苯甲酸相对分子质量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为___________ ,操作Ⅱ为___________ 。
(2)无色液体A是___________ ,定性检验A的试剂是___________ ,现象是___________ 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确,请完成表中内容。
(4)纯度测定:称取1.220g产品,配成100mL苯甲酸液,移取25.00mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol产品中苯甲酸质量分数为___________ (保留两位有效数字)
 +2KMnO4
+2KMnO4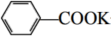 +2MnO2↓+H2O
+2MnO2↓+H2O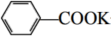 +HCl
+HCl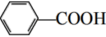 +KCl
+KCl实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。

已知:苯甲酸相对分子质量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为
(2)无色液体A是
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确,请完成表中内容。
| 序号 | 实验方案 | 实验现象 | 实验结论 |
| ① | 将白色固体B加入水中,加热溶解,冷却结晶、过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液 | 生成 | 滤液含Cl- |
| ③ | 干燥白色晶体,测定熔点 | 白色晶体在 | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100mL苯甲酸液,移取25.00mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol产品中苯甲酸质量分数为
19-20高二下·云南曲靖·期中
类题推荐
苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。
反应原理:
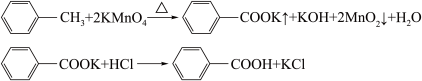
已知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
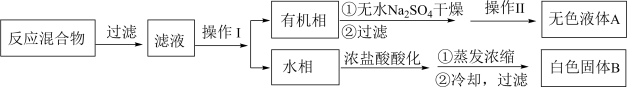
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
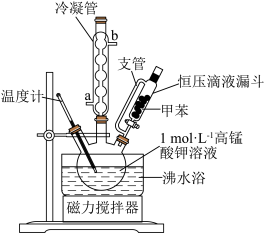
(1)图中冷凝管的进水口为___ (填“a”或“b”)。支管的作用是____ 。
(2)在本实验中,三颈烧瓶最合适的容积_____ (填字母)。
A.50mL B.100mL C.200mL D.250mL
相对于用酒精灯直接加热,用沸水浴加热的优点是_____ 。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
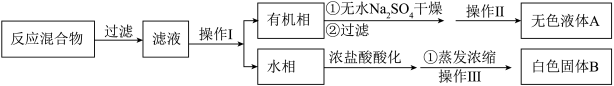
(3)操作Ⅰ的名称是____ ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是______ 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。
请完成表中内容。
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______ (填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______ 。
反应原理:

已知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。

(1)图中冷凝管的进水口为
(2)在本实验中,三颈烧瓶最合适的容积
A.50mL B.100mL C.200mL D.250mL
相对于用酒精灯直接加热,用沸水浴加热的优点是
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯

(3)操作Ⅰ的名称是
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。
请完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体加入水中,加热溶解, | 得到白色晶体和无色溶液 | |
| ② | 取少重滤液于试管中, | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, | 白色晶体是苯甲酸 |
| 第一次 | 第二次 | 第三次 | 第四 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网