解答题-实验探究题 适中0.65 引用4 组卷318
已知:
回答下列问题:
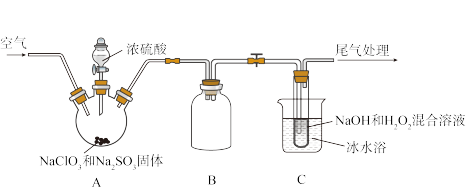
(1)
(2)装置A中所发生反应的化学方程式为
(3)装置C中盛装的试剂是
(4)分析发现该装置有不足之处,改进的方法是
(5)为测定某
①确称取
②取
21-22高三上·贵州贵阳·开学考试
类题推荐
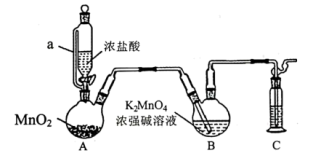
实验室用Cl2氧化K2MnO4来制备KMnO4,装置如图1所示:

已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO +2H2O=2MnO
+2H2O=2MnO +MnO2↓+4OH-。
+MnO2↓+4OH-。
请回答下列问题:
(1)K2MnO4中锰元素的化合价为___________ 价。
(2)装置B中生成KMnO4的离子方程式为___________ 。
(3)进入装置B的Cl2中含有杂质HCl,HCl___________ (填“需要”或“不需要”)除去,理由是___________ 。
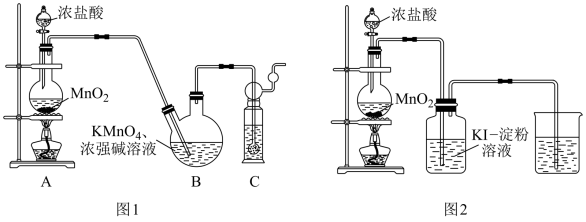
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示
根据第一组、第二组的实验可得出的结论是___________ ,根据第三组实验可得出的结论是___________ 。
(5)为测定某NaHSO3固体的纯度,现用0.1000mol·L-1的酸性KMnO4溶液进行滴定。(已知: )
)
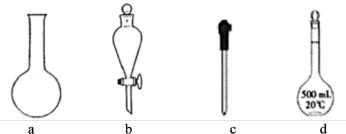
①称取Wg NaHSO3固体溶于水配成100mL溶液,下列仪器在该过程中肯定不需要用到的是___________ (填仪器名称)。

②取25.00mL NaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为___________ 。

已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO
请回答下列问题:
(1)K2MnO4中锰元素的化合价为
(2)装置B中生成KMnO4的离子方程式为
(3)进入装置B的Cl2中含有杂质HCl,HCl
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示
| 组别 | 反应条件 | 盐酸浓度 | 淀粉-KI溶液的颜色变化 |
| 第一组 | 微热 | 10mol·L-1 | 变蓝色 |
| 第二组 | 常温 | 10mol·L-1 | 不变色 |
| 第三组 | 微热 | 5mol·L-1 | 不变色 |
(5)为测定某NaHSO3固体的纯度,现用0.1000mol·L-1的酸性KMnO4溶液进行滴定。(已知:
①称取Wg NaHSO3固体溶于水配成100mL溶液,下列仪器在该过程中肯定不需要用到的是

②取25.00mL NaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为
实验室用Cl2氧化K2MnO4来制备KMnO4,装置如图1所示:
已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO + 2H2O=2
+ 2H2O=2 +MnO2↓+4OH-。
+MnO2↓+4OH-。
请回答下列问题:。
(1)K2 MnO4中锰元素的化合价为___________ 价。
(2)装置B中生成KMnO4的离子方程式为___________
(3)进入装置B的Cl2中含有杂质HCl,HCl___________ (填“ 需要”或“不需要”)除去,理由是___________ 。
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示:
根据第一组、第二组的实验可得出的结论是___________ ,根据第 三组实验可得出的结论是___________ 。
(5)为测定某NaHSO3固体的纯度,现用0. 1000 mol·L-1的酸性KMnO4溶液进行滴定。(已知: 2 +5
+5 +H+=2Mn2+ +5
+H+=2Mn2+ +5 +3H2O)
+3H2O)
①称取W g NaHSO3固体溶于水配成100 mL溶液,下列仪器在该过程中肯定不需要用到的是___________ (填仪器名称)。
a. b.
b.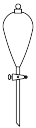 c.
c.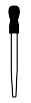 d.
d.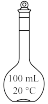
②取25.00mLNaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为。___________ ,NaHSO3固体的纯度为___________ (用含V 和W的代数式表示)。

已知:K2MnO4在浓强碱溶液中可稳定存在,碱性减弱时易发生反应3MnO
请回答下列问题:。
(1)K2 MnO4中锰元素的化合价为
(2)装置B中生成KMnO4的离子方程式为
(3)进入装置B的Cl2中含有杂质HCl,HCl
(4)甲同学设计如图2所示的实验来研究二氧化锰与盐酸的反应情况,各组实验参数如表所示:
| 组别 | 反应条件 | 盐酸浓度 | 淀粉—KI溶液的颜色变化 |
| 第一组 | 微热 | 10mol/L | 变蓝色 |
| 第二组 | 常温 | 10mol/L | 不变色 |
| 第三组 | 微热 | 5mol/L | 不变色 |
(5)为测定某NaHSO3固体的纯度,现用0. 1000 mol·L-1的酸性KMnO4溶液进行滴定。(已知: 2
①称取W g NaHSO3固体溶于水配成100 mL溶液,下列仪器在该过程中肯定不需要用到的是
a.
 b.
b.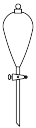 c.
c.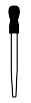 d.
d.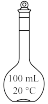
②取25.00mLNaHSO3溶液置于锥形瓶中,用酸性KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。滴定终点的现象为。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网