单选题 较难0.4 引用17 组卷2620
在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH= -164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= 41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)=CO2(g)+CH4(g) ΔH= -247.1 kJ/mol
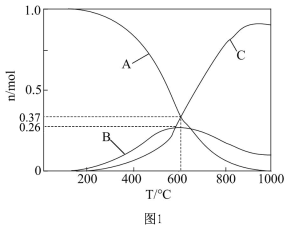
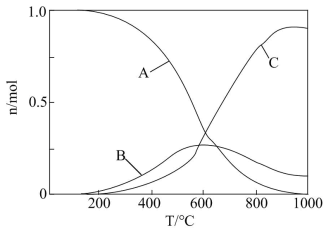
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法正确的是
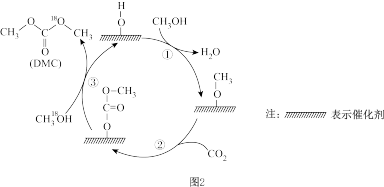
反应Ⅰ:CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH= -164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH= 41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)=CO2(g)+CH4(g) ΔH= -247.1 kJ/mol
向恒压、密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法正确的是

| A.反应Ⅰ的平衡常数可表示为K= |
| B.图中曲线B表示CO的物质的量随温度的变化 |
| C.提高 CO2转化为CH4的转化率,需要研发在低温区高效的催化剂 |
| D.CH4(g)+H2O(g) =CO(g)+3H2(g)的ΔH= -205.9 kJ/mol |
2021高三·全国·专题练习
类题推荐
二氧化碳加氢制甲烷过程中的主要反应为:
反应Ⅰ:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1=-164.7 kJ·mol–1
CH4(g)+2H2O(g) ΔH1=-164.7 kJ·mol–1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2 kJ·mol–1
CO(g)+H2O(g) ΔH2=+41.2 kJ·mol–1
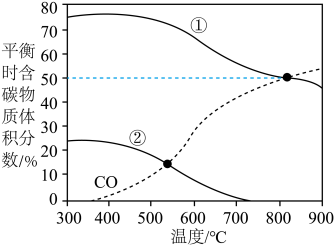
在1.01×105Pa恒压条件下,按n起始(CO2):n起始(H2)=1:1投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
反应Ⅰ:CO2(g)+4H2(g)
反应Ⅱ:CO2(g)+H2(g)
在1.01×105Pa恒压条件下,按n起始(CO2):n起始(H2)=1:1投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所示。下列说法正确的是
| A.2CO(g)+2H2(g) |
| B.曲线①表示平衡时CH4的体积分数随温度的变化 |
| C.一定温度下,选用高效催化剂能提高平衡时甲烷的产率 |
| D.温度在200~300℃时,CO2在平衡体系中的分压增大 |
CO2催化加氢是碳中和的重要手段之一,以下是CO2加氢时发生的两个主要反应:
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中 和
和 随温度变化关系如图所示。
随温度变化关系如图所示。
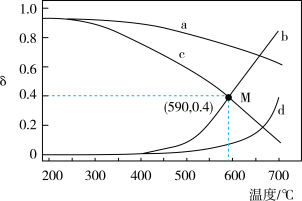
下列有关说法正确的是
反应I:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g) ΔH1=-165.0 kJ·mol-1
反应II:CO2(g)+H2(g) ⇌CO(g)+H2O(g) ΔH2
在体积为VL的两个恒容密闭容器中,分别按表所示充入一定量的CO2和H2.平衡体系中
| 容器 | 起始物质的量/mol | |
| CO2 | H2 | |
| 甲 | 0.1 | 0.3 |
| 乙 | 1 | 3 |

下列有关说法正确的是
| A.ΔH2<0 |
| B.曲线b表示乙容器中 |
| C.M点对应H2的总转化率为66.7% |
| D.590℃条件下反应10min,某容器中 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网