解答题-原理综合题 适中0.65 引用2 组卷398
平衡思想是化学研究的一个重要观念。电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①常温下,物质的量浓度相同的三种溶液:a. 、b.
、b. 、c.
、c. ,
, 由大到小的顺序是
由大到小的顺序是_______ (填序号)。
②室温下, 溶液
溶液 ,用离子方程式表示溶液呈碱性的原因是
,用离子方程式表示溶液呈碱性的原因是_______ ,溶液中
_______ 。
(2)室温下,用 盐酸滴定
盐酸滴定 的氨水,滴定曲线如图所示。
的氨水,滴定曲线如图所示。
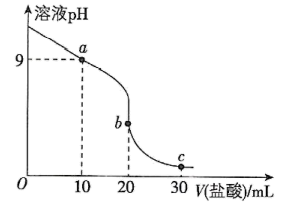
①a点所示的溶液中粒子浓度由大到小的顺序依次为_______ 
_______  。
。
②c点所示的溶液中
_______  (忽略溶液体积的变化)。
(忽略溶液体积的变化)。
(3)室温下, 、
、 的电离平衡常数分别为
的电离平衡常数分别为 、
、 。下列溶液混合后,
。下列溶液混合后, 大于7的是
大于7的是_______ (填序号)。
① 的盐酸和
的盐酸和 的
的 溶液等体积混合
溶液等体积混合
②等浓度、等体积 溶液、
溶液、 溶液混合
溶液混合
③ 的盐酸和
的盐酸和 的氨水等体积混合
的氨水等体积混合
④ 的醋酸溶液和
的醋酸溶液和 溶液等体积混合
溶液等体积混合
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | |||
| 电离常数(25℃) |
②室温下,
(2)室温下,用

①a点所示的溶液中粒子浓度由大到小的顺序依次为
②c点所示的溶液中
(3)室温下,
①
②等浓度、等体积
③
④
20-21高二·全国·单元测试
知识点:弱电解质在水溶液中的电离平衡盐类水解规律理解及应用盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理盐溶液中离子浓度大小的比较 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题.
(1)已知部分弱酸的电离常数如表:
① 溶液和
溶液和 溶液中,
溶液中,
______________  (填“>”、“<”或=”)
(填“>”、“<”或=”)
②常温下, 相同的三种溶液:a.
相同的三种溶液:a. b.
b. c.
c. ,其物质的量浓度由大到小的顺序是
,其物质的量浓度由大到小的顺序是______________ (填编号).
③室温下,一定浓度的 溶液
溶液 ,用离子方程式表示溶液呈碱性的原因是
,用离子方程式表示溶液呈碱性的原因是______________ ,溶液中
______________ .
(2)某温度下, 的盐酸中
的盐酸中 .该温度下,
.该温度下, 的
的 与
与 的
的 混合后
混合后 变为9,则硫酸与氢氧化钠的体积比为
变为9,则硫酸与氢氧化钠的体积比为______________ .
(3)室温下,用 盐酸溶液滴定
盐酸溶液滴定 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积).
的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积).______________ .
ⅱ. 点所示的溶液中
点所示的溶液中
______________ (写出准确值).
(1)已知部分弱酸的电离常数如表:
| 弱酸 | |||
| 电离常数 |
②常温下,
③室温下,一定浓度的
(2)某温度下,
(3)室温下,用
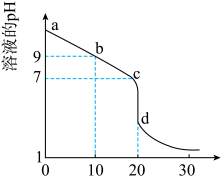
ⅱ.
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
① 溶液和
溶液和 溶液中,
溶液中,
_____ 
②常温下,物质的量浓度相同的三种溶液:A. B.
B. C.
C. ,其pH由大到小的顺序是
,其pH由大到小的顺序是_____ (填编号)。
③将少量 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是_____
④室温下,一定浓度的 溶液pH=9,用离子方程式表示溶液呈碱性的原因是
溶液pH=9,用离子方程式表示溶液呈碱性的原因是_____ ,溶液中
_____ (写出准确数值)
(2)某温度下,pH=3的盐酸中 该温度下,pH=2的
该温度下,pH=2的 与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为
与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为_____ 。
(3)室温下,用 盐酸溶液滴定
盐酸溶液滴定 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

d点所示的溶液中离子浓度由大到小的顺序依次为_____ 。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | |||
| 电离常数(25℃) |
②常温下,物质的量浓度相同的三种溶液:A.
③将少量
④室温下,一定浓度的
(2)某温度下,pH=3的盐酸中
(3)室温下,用

d点所示的溶液中离子浓度由大到小的顺序依次为
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如表:
①0.1mol/LNaCN溶液和0.1mol/LCH3COONa溶液中,
______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
②常温下,物质的量浓度相同的三种溶液:A. CH3COONa B. NaCN C. Na2CO3,其pH由大到小的顺序是______ (填编号)。
③将少量CO2通入NaCN溶液,反应的离子方程式是______ 。
④室温下,一定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______ ,溶液中c(CH3COO-)/c(CH3COOH) =______ 。
(2)常温下,向20.00mL0.1000mol/L的醋酸溶液中逐滴加入0.1000mol/L的NaOH溶液,pH值随NaOH溶液体积的变化如图所示。

①d点(NaOH溶液为20mL时)所示的溶液中离子浓度由大到小的顺序依次为______ 。
②b点所示的溶液中c(CH3COO-)-c(CH3COOH)=______ (写表达式)。
(1)已知部分弱酸的电离常数如表:
| 弱酸 | |||
| 电离常数(25℃) |
②常温下,物质的量浓度相同的三种溶液:A. CH3COONa B. NaCN C. Na2CO3,其pH由大到小的顺序是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,一定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)常温下,向20.00mL0.1000mol/L的醋酸溶液中逐滴加入0.1000mol/L的NaOH溶液,pH值随NaOH溶液体积的变化如图所示。

①d点(NaOH溶液为20mL时)所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(CH3COO-)-c(CH3COOH)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


