解答题-原理综合题 较易0.85 引用3 组卷486
按照要求书写方程式。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:____________________________________ ;
用化学方程式表示用石膏降低其碱性的反应原理:_________________________________ 。
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:___________________________________________ 。
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:_________________________________ 。
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:_____________________________________________ 。
(1)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
用离子方程式表示盐碱地产生碱性的原因:
用化学方程式表示用石膏降低其碱性的反应原理:
(2)SOCl2是一种液态化合物。向盛有10 ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。
请写出SOCl2与水反应的化学方程式:
(3)铅蓄电池是最常见的二次电池,使用方便,安全可靠,在生活中有广泛的应用。
请写出铅蓄电池放电时电池反应的离子方程式:
(4)制备像钠、镁、铝这样活泼的金属,电解法几乎是唯一可行的工业方法。
请写出工业上冶炼铝的化学方程式:
20-21高二上·重庆沙坪坝·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 H2+NiO(OH)
H2+NiO(OH) 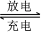 Ni(OH)2。电池放电时, 负极的电极反应式为
Ni(OH)2。电池放电时, 负极的电极反应式为

