多选题 较难0.4 引用1 组卷84
现有150mLNH4Cl-Na2SO4混合溶液,总质量为185g,其中有30gNH4Cl、40gNa2SO4,欲对其进行处理以得到NH4Cl。已知一些物质的溶解度(g/100gH2O)如下:
*溶解度数据按100克水中溶解Na2SO4的克数计。下列说法正确的是
| 温度/°C | 0 | 10 | 20 | 30 | 32.4 | 40 | 60 | 90 | 100 |
| NH4Cl | 29.7 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 71.3 | 77.3 | |
| Na2SO4·10H2O* | 4.9 | 9.1 | 19.5 | 41.0 | |||||
| Na2SO4 | 48.8 | 45.3 | 42.7 | 42.5 | |||||
| NaCl | 35.7 | 35.8 | 36.0 | 36.2 | 36.5 | 37.3 | 38.6 | 39.2 | |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 88.0 | 99.2 | 103.3 |
| A.若在90°C左右加热,将溶液蒸发浓缩至100mL,此时会析出5.8gNa2SO4,和6.4gNaCl |
| B.若在90°C左右加热,将溶液蒸发浓缩至70mL,此时会析出10.1gNa2SO4、5.0gNH4Cl和15.8gNaCl |
| C.在90°C左右蒸发浓缩时应控制溶液为80mL,趁热过滤分离析出的Na2SO4,然后将滤液冷却结晶,在35°C左右过滤即可得到较纯净的NH4Cl |
| D.可将混合溶液冷却至0~10°C,充分析出Na2SO4·10H2O过滤分离,然后对滤液进行加热蒸发浓缩,控制好浓缩程度,冷却结晶,在35°C左右过滤即可到较纯净的NH4Cl |
2018高二·广东·竞赛
类题推荐
20.某厂以重晶石(有效成分是BaSO4)为主要原料制取Ba(OH)2·8H2O晶体的示意图如下:
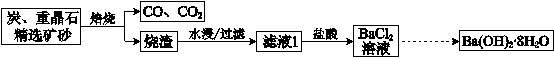
已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) ΔH1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g) ΔH2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
回答下列问题:
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=____kJ/mol。
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2·8H2O。
途径1:

①得到固体1的离子方程式是______。
②固体2与水反应的化学方程式是______。
途径2:
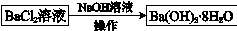
途径2中的“操作”是加热浓缩,冷却结晶,过滤。依据上述溶解度简表分析,过滤时的最佳温度是______;能从混合液中得到Ba(OH)2·8H2O晶体的原因是______。
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2·8H2O晶体和CuS的浊液,反应化学方程式是______。将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2·8H2O晶体。上述操作中趁热过滤的原因是______。

已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) ΔH1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g) ΔH2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
| 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | |
| Ba(OH)2·8H2O | 2.48 | 3.89 | 8.22 | 20.9 | 101 |
| NaOH | 98.0 | 109 | 129 | 174 | 314 |
| NaCl | 35.8 | 35.9 | 36.4 | 37.1 | 38.0 |
| BaCl2 | 33.5 | 35.8 | 40.8 | 46.2 | 52.5 |
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=____kJ/mol。
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2·8H2O。
途径1:

①得到固体1的离子方程式是______。
②固体2与水反应的化学方程式是______。
途径2:
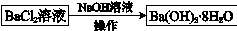
途径2中的“操作”是加热浓缩,冷却结晶,过滤。依据上述溶解度简表分析,过滤时的最佳温度是______;能从混合液中得到Ba(OH)2·8H2O晶体的原因是______。
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2·8H2O晶体和CuS的浊液,反应化学方程式是______。将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2·8H2O晶体。上述操作中趁热过滤的原因是______。
下面是某实验小组制备硫酸亚铁铵的原理:Fe(s)+2H+(aq)=Fe2++H2(g),Fe2+(aq)+2NH (aq)+2SO
(aq)+2SO (aq)+6H2O(l)=(NH4)2SO4·FeSO4·6H2O(s)。
(aq)+6H2O(l)=(NH4)2SO4·FeSO4·6H2O(s)。
已知三种盐的溶解度(单位为g/100gH2O)数据如下:
下列有关硫酸亚铁铵晶体的说法不正确的是
已知三种盐的溶解度(单位为g/100gH2O)数据如下:
| 温度 | FeSO4·7H2O | (NH4)2SO4 | (NH4)2SO4·FeSO4·6H2O |
| 10℃ | 20.0 | 73.0 | 17.2 |
| 20℃ | 26.5 | 75.4 | 21.6 |
| 30℃ | 32.9 | 78.0 | 28.1 |
| A.称取一定质量铁屑放入小烧杯中,加入蒸馏水煮沸,洗涤铁屑表面油污 |
| B.往盛有洁净铁屑的小烧杯中加入15 mL 3 mol·L-1H2SO4溶液,放在石棉网上小火煮沸,充分反应后,分离出未反应的铁粉,吸水后称重 |
| C.根据计算,称取所需固体(NH4)2SO4的用量,在室温下配制成饱和溶液,倒入制得的FeSO4溶液中 |
| D.控制一定条件,在水浴锅上蒸发浓缩至溶液表面刚出现薄层的结晶时,取下蒸发皿,放置、冷却,即有硫酸亚铁铵晶体析出 |
下表列出了KNO3与NaCl在不同温度时的溶解度:
(1)现有含123 g KNO3与17.9 g NaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(不考虑水的额外损失)。
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100 ℃并恒温蒸发浓缩;
③将溶液降温至10 ℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥。
A.在步骤②中,为确保没有晶体析出,溶液中至少要保留________ g水;
B.在步骤③中,最多可得到KNO3晶体________ g;
C.除去KNO3中少量NaCl的主要实验流程可用下图表示:
 ;
;____________
D.洗涤时,应选用少量________ (选填“热水”或“冷水”),其目的是____________ ,证明已经洗涤干净的方法是________ 。
(2)除去NaCl中少量KNO3的方法是:先将NaCl和KNO3混合物置于适量水中,加热搅拌保证固体能全部溶解,后蒸发溶液至有大量晶体析出时停止,再趁热过滤,并对过滤所得NaCl晶体进行洗涤和干燥。上述方法中,趁热过滤的目的是____________
(3)取23.4 g NaCl和40.4 g KNO3,加70 g水,加热溶解。在100 ℃时蒸发掉50 g水,维持该温度过滤,得到的晶体质量为________ g;将滤液冷却至10 ℃,充分结晶,写出析出晶体的化学式______________ 。
| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| KNO3的溶解度(g) | 13.3 | 20.9 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl的溶解度(g) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(1)现有含123 g KNO3与17.9 g NaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(不考虑水的额外损失)。
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100 ℃并恒温蒸发浓缩;
③将溶液降温至10 ℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥。
A.在步骤②中,为确保没有晶体析出,溶液中至少要保留
B.在步骤③中,最多可得到KNO3晶体
C.除去KNO3中少量NaCl的主要实验流程可用下图表示:
 ;
;D.洗涤时,应选用少量
(2)除去NaCl中少量KNO3的方法是:先将NaCl和KNO3混合物置于适量水中,加热搅拌保证固体能全部溶解,后蒸发溶液至有大量晶体析出时停止,再趁热过滤,并对过滤所得NaCl晶体进行洗涤和干燥。上述方法中,趁热过滤的目的是
(3)取23.4 g NaCl和40.4 g KNO3,加70 g水,加热溶解。在100 ℃时蒸发掉50 g水,维持该温度过滤,得到的晶体质量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


