单选题 适中0.65 引用2 组卷317
甲醇既是重要的化工原料,也是性能优良的能源和车用燃料。利用煤气过程中生成的CO和 可制备甲醇:
可制备甲醇:
 ,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和
,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和 ,测得部分相关物质的浓度随时间的变化如图乙所示。
,测得部分相关物质的浓度随时间的变化如图乙所示。
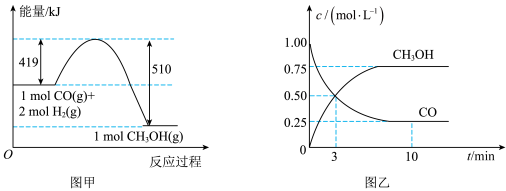
下列有关说法正确的是

下列有关说法正确的是
| A.该反应的 | B.前3 min内 |
| C.氢气的平衡转化率为75% | D.该反应的平衡常数 |
20-21高二·全国·课时练习
类题推荐
利用CO和H2在催化剂的作用下合成甲醇,发生如下反应:CO(g)+2H2(g) CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
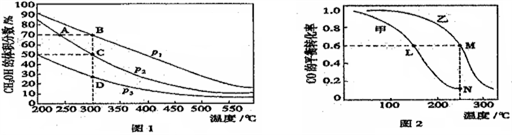
 CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
| A.该反应的ΔH> 0; P1> P2 | B.反应速率B点高于D点 |
| C.A、C两点的平衡常数相同 | D.M、L两点中,CH3OH的体积分数相同,且p(M)= 2p(L) |
甲醇是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式及其在不同温度下的化学平衡常数如表所示。
(1)下列措施能使反应③的平衡体系中 增大的是
增大的是__
A.将H2O(g)从体系中分离出去 B.恒容时充入He(g),使体系压强增大
C.升高温度 D.恒容时再充入1molH2(g)
(2)T℃时,反应③在恒容密闭容器中充入1molCO2和nmolH2,混合气体中CH3OH的体积分数与氢气的物质的量的关系如图1所示。图1中A、B、C三点对应的体系,CO2的转化率最大的是___ (填字母)。

(3)工业上也用合成气(H2和CO)合成甲醇,反应为2H2(g)+CO(g) CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和CO物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和CO物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
①图2中S代表的物理量是___ 。
②300℃时,氢气的物质的量随时间变化如表所示
在该温度下,上述反应的平衡常数为___ 。若再向该平衡体系中再加入2molCO、2molH2、2molCH3OH,保持温度和容器体积不变,则平衡会___ (填“正向移动”“逆向移动”或“不移动”)。
| 化学反应 | 化学平衡常数 | 温度(℃) | ||
| 500 | 700 | 800 | ||
| ①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
| ②H2(g)+CO2(g) | K2 | 1.0 | 1.70 | 2.52 |
| ③3H2(g)+CO2(g) | K3 | |||
A.将H2O(g)从体系中分离出去 B.恒容时充入He(g),使体系压强增大
C.升高温度 D.恒容时再充入1molH2(g)
(2)T℃时,反应③在恒容密闭容器中充入1molCO2和nmolH2,混合气体中CH3OH的体积分数与氢气的物质的量的关系如图1所示。图1中A、B、C三点对应的体系,CO2的转化率最大的是

(3)工业上也用合成气(H2和CO)合成甲醇,反应为2H2(g)+CO(g)
①图2中S代表的物理量是
②300℃时,氢气的物质的量随时间变化如表所示
| 反应时间/min | 0 | 1 | 4 | 5 |
| H2/mol | 8 | 5.4 | 4 | 4 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网