填空题 适中0.65 引用2 组卷579
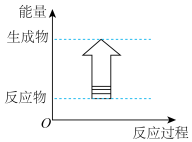
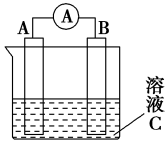
(1)利用8NH3+6NO2=7N2+12H2O可以消除氮氧化物的污染,若设计成原电池,使用2mol·L-1的KOH溶液为电解质溶液。该电池正极的电极反应式为_______ ,放电一段时间后,负极附近溶液pH将_______ (填“增大”、“减小”或“不变”)。
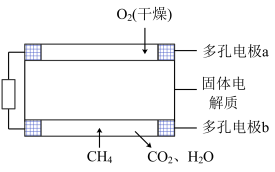
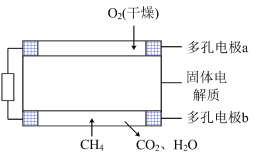
(2)一种熔融碳酸盐燃料电池原理示意如图所示
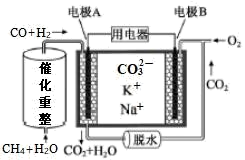
①写出催化重整的化学方程式_______ 。
②电池工作时, 向
向_______ (填A或B)极移动,电极A上H2参与的电极反应为:_______ 。
③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为_______ L。
(2)一种熔融碳酸盐燃料电池原理示意如图所示

①写出催化重整的化学方程式
②电池工作时,
③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为
20-21高一下·江西宜春·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网