解答题-原理综合题 适中0.65 引用1 组卷208
(1)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
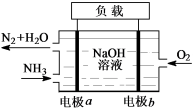
①电极a名称是___________ 。
②电解质溶液中OH-离子向___________ 移动(填“电极a”或 “电极b”)。
③电极b的电极反应式为___________ 。
④可以通过NH3跟NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学方程式为___________ 。
(2)利用甲烷催化还原氮氧化物,可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H =-574 kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H =-1160 kJ/mol
③H2O(l)=H2O(g) △H = +44 kJ/mol
写出CH4将NO2还原为N2并生成液态水时的热化学方程式___________ 。
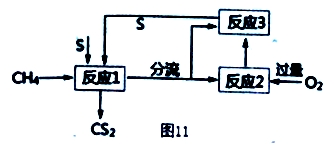
(3)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为___________ 。为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为___________ 。


①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
④可以通过NH3跟NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学方程式为
(2)利用甲烷催化还原氮氧化物,可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H =-574 kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H =-1160 kJ/mol
③H2O(l)=H2O(g) △H = +44 kJ/mol
写出CH4将NO2还原为N2并生成液态水时的热化学方程式
(3)科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为

20-21高一下·辽宁铁岭·期末
类题推荐
氮氧化物(NO2)是一种主要的大气污染物,必须进行处理。
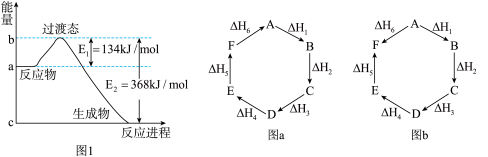
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①△H1___ 0,△H3____ 0。(填“>”或“<”)
②N2(g)+O2(g)=2NO(g)△H=____ kJ·mol-1。
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为_______ 。
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:
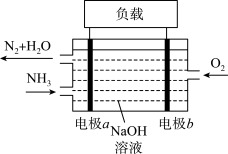
①电极a名称是______ 。
②电解质溶液中OH-离子向_____ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为_____ 。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是_____ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | △H1 | △H2 | △H3 |
| 热量值kJ/mol | 945 | 498 | 630 |
①△H1
②N2(g)+O2(g)=2NO(g)△H=
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网