单选题 适中0.65 引用3 组卷348
海水开发利用的部分过程如图所示,下列有关说法正确的是
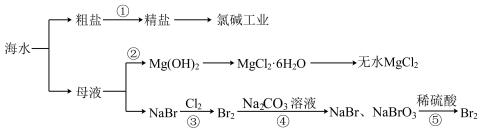

| A.除去粗盐中的Ca2+、Mg2+、 |
| B.步骤②在工业生产中常选用石灰乳作Mg2+的沉淀剂 |
| C.第④步反应中氧化产物与还原产物的物质的量之比为5:1 |
| D.第⑤步反应的离子方程式为: |
20-21高一下·四川成都·期末
类题推荐
海水开发利用的部分过程如图所示,下列有关说法错误的是
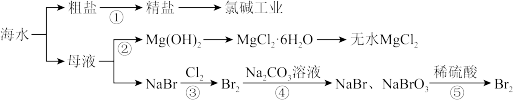
| A.由粗盐制取精盐,需除去其中的不溶性杂质与可溶性杂质 |
| B.步骤②在工业生产中常加入生石灰作Mg2+的沉淀剂,以降低生产成本 |
| C.第④步反应的化学方程式为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ |
| D.第⑤步反应中理论上生成1molBr2时,转移电子数为2NA |
海水开发利用的部分过程如图所示,下列有关说法错误的是
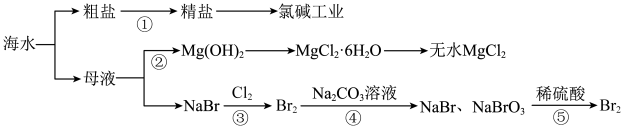

| A.由粗盐制取精盐,需除去其中的不溶性杂质与可溶性杂质 |
| B.步骤②在工业生产中常加入火碱作Mg2+的沉淀剂,以降低生产成本 |
| C.第④步反应的化学方程式为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ |
| D.第⑤步反应中理论上生成1molBr2时,转移电子数为5NA |
根据海水综合利用的工业流程图,判断下列说法正确的是
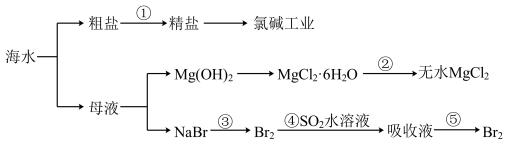

| A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.过程③中可以选择氯气作氧化剂 |
| D.第④步反应的离子方程式为:Br2+SO2+2H2O=2H++SO42-+2HBr |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


