解答题-原理综合题 适中0.65 引用1 组卷186
(1)已知该反应在反应过程中体系温度会升高,且每摩尔
(2)一定温度下,向体积为2L的刚性密闭容器中充入
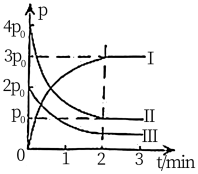
①图中表示
②
③能说明上述反应已达到平衡状态的是
a.容器内
b.
c.容器中气体的密度不随时间而变化
d.容器内压强不随时间面变化
20-21高一下·河北石家庄·期末
类题推荐
H2作为重要的化工原料及清洁能源,一直备受关注。请回答下列问题:
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)下表为部分化学键的键能(键能:断开1 mol化学键所需的热量):
每有1 mol N2参与人工固氮,会_______ (填“吸收”或“放出”)的能量为_______ kJ。
(2)一定温度下,向体积为1 L的刚性密闭容器中充入0.1 mol N2和0.3 mol H2,发生反应:N2(g)+3H2(g) 2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:
2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:

①0~2min内,用NH3表示该反应的速率为___________ mol·L-1·min-1。
②N2的转化率为___________ 。
③能说明上述反应已达到平衡状态的是___________ (填选项字母)。
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
II.氢能源的利用。氢氧燃料碱性电池工作原理如图。
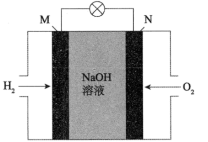
①M极为___________ (填“正极”或“负极”)。
②N极上发生反应的电极反应式为______________ 。
③电池工作时,当外电路中流过0.2 mol电子时,消耗氧气在标准状况下的体积为_____ L。
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g)
(1)下表为部分化学键的键能(键能:断开1 mol化学键所需的热量):
| 化学键 | H-H | N-H | |
| 键能/(kJ | 946 | 436 | 391 |
每有1 mol N2参与人工固氮,会
(2)一定温度下,向体积为1 L的刚性密闭容器中充入0.1 mol N2和0.3 mol H2,发生反应:N2(g)+3H2(g)

①0~2min内,用NH3表示该反应的速率为
②N2的转化率为
③能说明上述反应已达到平衡状态的是
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
II.氢能源的利用。氢氧燃料碱性电池工作原理如图。

①M极为
②N极上发生反应的电极反应式为
③电池工作时,当外电路中流过0.2 mol电子时,消耗氧气在标准状况下的体积为
H2作为重要的化工原料及清洁能源,一直备受关注。请回答下列问题:
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g)⇌2NH3(g)。
(1)下表为部分化学键的键能(键能:断开1mol化学键所需的热量):
每有0.5molN2参与人工固氮,_______ (填“吸收”或“放出”)的能量为_______ kJ。
(2)一定温度下,向体积为1L的刚性密闭容器中充入0.1molN2和0.3molH2,发生反应:N2(g)+3H2(g)⇌2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:

①0~2min内,用NH3表示该反应的速率为_______ mol·L-1·min-1。
②N2的转化率为_______ 。
③能说明上述反应已达到平衡状态的是_______ (填选项字母)。
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
Ⅱ.氢能源的利用。氢氧燃料碱性电池工作原理如图。
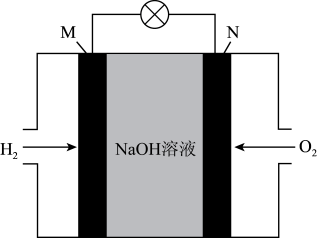
(3)M极为_______ (填“正极”或“负极”)。
(4)N极上发生反应的电极反应式为_______ 。
(5)电池工作时,当外电路中流过0.2mol电子时,消耗氧气在标准状况下的体积为_______ L。
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g)⇌2NH3(g)。
(1)下表为部分化学键的键能(键能:断开1mol化学键所需的热量):
| 化学键 | N≡N | H-H | N-H |
| 键能(kJ∙mol-1) | 946 | 436 | 391 |
(2)一定温度下,向体积为1L的刚性密闭容器中充入0.1molN2和0.3molH2,发生反应:N2(g)+3H2(g)⇌2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:

①0~2min内,用NH3表示该反应的速率为
②N2的转化率为
③能说明上述反应已达到平衡状态的是
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
Ⅱ.氢能源的利用。氢氧燃料碱性电池工作原理如图。

(3)M极为
(4)N极上发生反应的电极反应式为
(5)电池工作时,当外电路中流过0.2mol电子时,消耗氧气在标准状况下的体积为
氮的化合物在工农业生产中有着重要作用。回答下列问题:
(1)氮的固定对人类生存至关重要,下列过程属于固氮过程的是___________(填选项字母)。
(2)实验室可用稀硝酸检验黄金的真假(假黄金为铜合金),若是假黄金则出现的现象为___________ ,铜与稀硝酸反应的离子方程式为___________ 。
(3)一定温度下,向某0.3L刚性密闭容器中加入一定量的 、
、 和
和 ,发生反应:
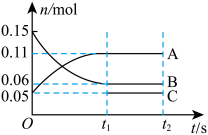
,发生反应: 。反应过程中各物质的物质的量随时间变化关系如图所示:
。反应过程中各物质的物质的量随时间变化关系如图所示:___________ (填化学式),起始时加入的C的物质的量为___________ °
②0~ s内,用
s内,用 表示该反应的化学反应速率为
表示该反应的化学反应速率为___________ 。
③下列措施能增大该反应的正反应速率的是___________ (填选项字母)。
A.向容器中加入高效催化剂 B.通过向容器中通入少量He,增大压强
C.从体系中适当分离出少量 D.适当升高容器中的反应温度
D.适当升高容器中的反应温度
④不能说明上述反应已达到平衡状态的是___________ (填选项字母)。
A.容器内 的浓度保持不变 B.
的浓度保持不变 B.
C.混合气体的密度保持不变 D.容器中气体的平均相对分子质量不随时间而变化
(1)氮的固定对人类生存至关重要,下列过程属于固氮过程的是___________(填选项字母)。
| A.将氨气转化为氯化铵的过程 | B.将氮气转化为氨气的过程 |
| C.植物将硝酸铵吸收的过程 | D.将氮气转化为氮化镁的过程 |
(2)实验室可用稀硝酸检验黄金的真假(假黄金为铜合金),若是假黄金则出现的现象为
(3)一定温度下,向某0.3L刚性密闭容器中加入一定量的
②0~
③下列措施能增大该反应的正反应速率的是
A.向容器中加入高效催化剂 B.通过向容器中通入少量He,增大压强
C.从体系中适当分离出少量
④不能说明上述反应已达到平衡状态的是
A.容器内
C.混合气体的密度保持不变 D.容器中气体的平均相对分子质量不随时间而变化
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


