解答题-实验探究题 适中0.65 引用2 组卷290
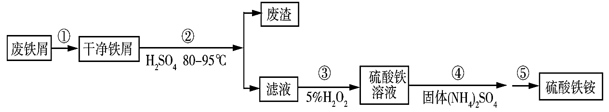
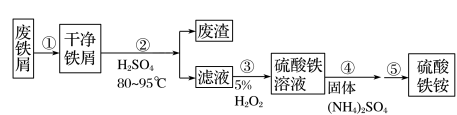
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:
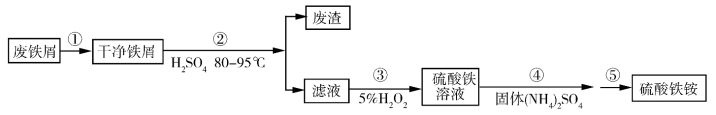
回答下列问题:
(1)步骤①的操作中用热的饱和Na2CO3溶液浸泡废铁屑,目的是_______ 。
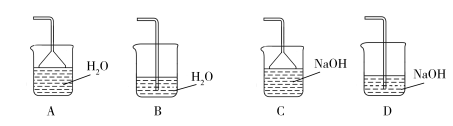
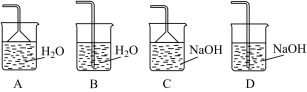
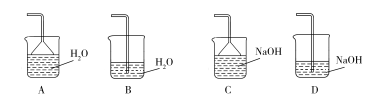
(2)步骤②加快化学反应速率的方法有_______ ;温度保持80~95 ℃,采用的合适加热方式是_______ ;铁屑中含有少量硫化物杂质,反应产生的气体需要净化处理,合适的装置为_______ (填标号)。
(3)步骤③中发生的离子反应方程式_______ ,步骤⑤蒸发浓缩时温度不宜过高,否则产率会降低,产品不纯。原因是_______ 。
(4)用冷水洗涤硫酸铁铵晶体的操作是_______ 。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉2个结晶水,失重8.41%。硫酸铁铵晶体的化学式为_______ 。

回答下列问题:
(1)步骤①的操作中用热的饱和Na2CO3溶液浸泡废铁屑,目的是
(2)步骤②加快化学反应速率的方法有

(3)步骤③中发生的离子反应方程式
(4)用冷水洗涤硫酸铁铵晶体的操作是
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉2个结晶水,失重8.41%。硫酸铁铵晶体的化学式为
20-21高二下·江苏南京·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网