解答题-原理综合题 适中0.65 引用1 组卷44
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______ 。
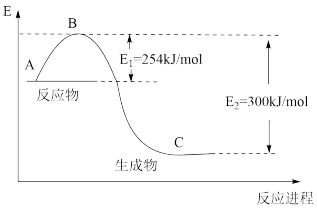
(2)若已知表中数据:
试根据表中及图中数据计算N-H的键能:_______ kJ·mol-1。
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。
已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-akJ·mol-1
② N2(g)+O2(g)=2NO(g) ΔH2=-bkJ·mol-1
则NH3还原NO的热化学方程式:_______ 。
(4)N、H、O元素形成的离子化合物为_______ (填化学式)。
(5) 氨气可用电解法合成,其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图1和图2所示。
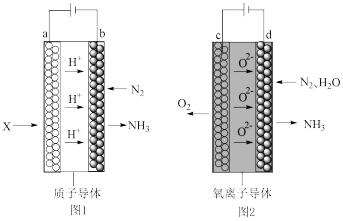
图1中,a 电极上通入的X 为_______ ;图 2 中,d 电极上的电极反应式为_______ 。
(1)图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:

(2)若已知表中数据:
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能:
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。
已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-akJ·mol-1
② N2(g)+O2(g)=2NO(g) ΔH2=-bkJ·mol-1
则NH3还原NO的热化学方程式:
(4)N、H、O元素形成的离子化合物为
(5) 氨气可用电解法合成,其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图1和图2所示。

图1中,a 电极上通入的X 为
20-21高一下·甘肃平凉·阶段练习
类题推荐
氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:____________________________________ 。
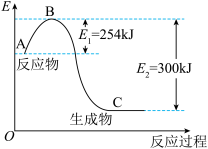
(2)已知化学键键能是形成或断裂1mol化学键放出或吸收的能量,单位为kJ·mol-1。
试根据表中及(1)的图中数据计算N—H键的键能为________ kJ·mol-1。
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)ΔH1=-akJ·mol-1①
N2(g)+O2(g)=2NO(g)ΔH2=-bkJ·mol-1②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=________ kJ·mol-1(用含a、b的式子表示)。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为____________ 。
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:

(2)已知化学键键能是形成或断裂1mol化学键放出或吸收的能量,单位为kJ·mol-1。
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)ΔH1=-akJ·mol-1①
N2(g)+O2(g)=2NO(g)ΔH2=-bkJ·mol-1②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为
回答下列问题:
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:_______ ;
(2)若已知下列数据:
试根据表中及图中数据计算N-H的键能_______ kJ• mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1_______ , 
_______ (填“增大”、“减小、” “不变”)。
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如




若1mol NH3还原NO至N2,则该反应过程中的反应热
_______ kJ/mol (用含a、b的式子表示)
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ • mol-1 | 435 | 943 |
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
若1mol NH3还原NO至N2,则该反应过程中的反应热
I.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出1 mol N2(g)和H2(g)反应的热化学方程式:___________ 。
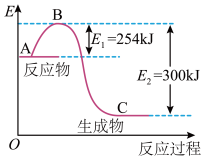
(2)若已知下列数据:
根据表中及图中数据计算N—H键的键能是___________ kJ·mol-1。
(3)用NH3催化还原NO,还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1 ①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ·mol-1 ②
求:若1 mol NH3还原NO至N2,则该反应过程中的反应热ΔH3=___________ kJ·mol-1(用含a、b的式子表示)。
II.2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
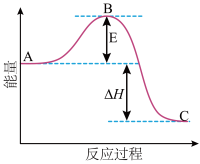
已知:1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1.请回答下列问题:
(4)E的大小对该反应的反应热___________ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___________ (填“升高”还是“降低”),△H___________ (填“变大”、“变小”或“不变”)。
(5)图中△H=___________ kJ·mol-1。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出1 mol N2(g)和H2(g)反应的热化学方程式:

(2)若已知下列数据:
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
(3)用NH3催化还原NO,还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1 ①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ·mol-1 ②
求:若1 mol NH3还原NO至N2,则该反应过程中的反应热ΔH3=
II.2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。

已知:1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1.请回答下列问题:
(4)E的大小对该反应的反应热
(5)图中△H=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


