解答题-实验探究题 较难0.4 引用2 组卷328
亚硫酸钠(Na2SO3)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 Na2SO3的性质,进行了如下实验。
【性质预测】
(1)Na2SO3中硫元素的化合价是_______ ,属于S元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下,KMnO4 被还原为无色的 Mn2+。
【分析解释】
(2)实验ⅰ中,反应的离子方程式是_______ 。
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是_______ 。
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO 具有氧化性,可产生 S;
具有氧化性,可产生 S;
假设 b:空气中存在 O2,在酸性条件下,由于_______ (用离子方程式表示),可产生 S;
假设 c:酸性溶液中的 SO 具有氧化性,可产生 S。
具有氧化性,可产生 S。
②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入_______ (填试剂名称),产生有臭鸡蛋气味的气体,离子方程式为_______ ,溶液未变浑浊。
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:_______ 。
【性质预测】
(1)Na2SO3中硫元素的化合价是
【实验验证】
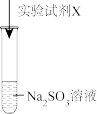 | 实验序号 | 实验试剂X | 实验现象 |
| ⅰ | KMnO4溶液、稀硫酸 | 紫色褪去,变为无色 | |
| ⅱ | Na2S 溶液、稀硫酸 | 加入Na2S溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊。 |
【分析解释】
(2)实验ⅰ中,反应的离子方程式是
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO
假设 b:空气中存在 O2,在酸性条件下,由于
假设 c:酸性溶液中的 SO
②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:
20-21高一下·甘肃平凉·阶段练习
类题推荐
某小组同学探究MnO 、MnO
、MnO 的性质。
的性质。
资料:i.MnO 的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能
的氧化能力与溶液的酸碱度有关,在酸性环境、中性环境、碱性环境能
被SO 分别还原为Mn2+(无色)、MnO2、MnO
分别还原为Mn2+(无色)、MnO2、MnO (绿色)。
(绿色)。
ii. MnO 在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO
在强碱溶液中能稳定存在,在酸性或纯水环境中易转化为MnO 和MnO2。
和MnO2。
I.验证MnO 与SO
与SO 的反应,实验如下:
的反应,实验如下:
(1)实验①参与反应的高锰酸钾和亚硫酸钠物质的量之比为_______ 。
(2)实验④中绿色很快消失,有大量棕色沉淀生成,结合离子方程式分析可能的原因_______ 。甲同学补做了实验_______ (填操作和现象),证明猜测合理。
II.验证 MnO 的性质。
的性质。
某同学用b试管得到的绿色溶液设计实验如下:
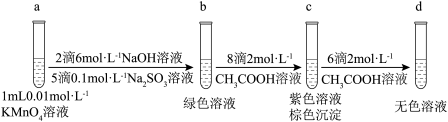
(3)c试管中得到紫色溶液和棕色浑浊的离子反应方程式为_______ 。继续滴加醋酸,沉淀溶解,得到无色透明溶液,有如下两种猜想:
① MnO 、MnO2可能被CH3COOH还原。
、MnO2可能被CH3COOH还原。
设计实验:将1mL 0.01mol·L−1 KMnO4溶液与少量MnO2固体混合,再向其中加入少许2mol·L−1 CH3COOH溶液,_______ (填现象),证明猜想不合理。
② MnO 、MnO2 可能被
、MnO2 可能被_______ 还原,发生的反应:_______ ,_______ 。
经实验验证,猜想合理。
由以上实验可知:MnO 、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
、MnO2的性质不仅与溶液的酸碱度有关;还与试剂的用量等有关。
资料:i.MnO
被SO
ii. MnO
I.验证MnO
| 实验 | 序号 | 试剂X | 现象 |
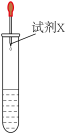 1mL0.01mol·L−1 KMnO4溶液 | ① | 2滴3mol·L−1 H2SO4 3滴0.1mol·L−1 Na2SO3 | 溶液褪为无色 |
| ② | 2滴纯水 3滴0.1mol·L−1 Na2SO3 | 产生棕色沉淀 | |
| ③ | 2滴6mol·L−1 NaOH 3滴0.1 mol·L−1 Na2SO3 | 溶液变为绿色 | |
| ④ | 2滴6mol·L−1 NaOH 10滴0.1mol·L−1 Na2SO3 | 溶液变为绿色溶液, 有浑浊,绿色很快消失,有大量棕色沉淀生成 |
(2)实验④中绿色很快消失,有大量棕色沉淀生成,结合离子方程式分析可能的原因
II.验证 MnO
某同学用b试管得到的绿色溶液设计实验如下:

(3)c试管中得到紫色溶液和棕色浑浊的离子反应方程式为
① MnO
设计实验:将1mL 0.01mol·L−1 KMnO4溶液与少量MnO2固体混合,再向其中加入少许2mol·L−1 CH3COOH溶液,
② MnO
经实验验证,猜想合理。
由以上实验可知:MnO
某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于___________ ,因此可以与某些碱反应。
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现___________ 性。
(3)预测FeCl2具有还原性,预测依据是___________ ,因此可以与酸性KMnO4溶液反应。
(4)进行如下实验操作:
①i中的现象是___________ ,用化学方程式表示产生该现象的原因:___________ 、___________ 。
②ii中反应的离子方程式是___________ 。
③iii中的现象是___________ 。
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②___________ , 为证实该反应中Fe2+确实被氧化,需要在反应后的溶液中加入试剂___________ ,观察到现象___________ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
(6)iv中反应的离子方程式是___________ 。
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(9)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________ 。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(3)预测FeCl2具有还原性,预测依据是
(4)进行如下实验操作:
 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②ii中反应的离子方程式是
③iii中的现象是
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 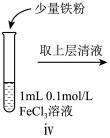 |  | 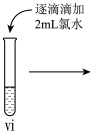 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色, 而后红色褪去 |
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(9)进一步预测SCN-可能被转化为SO
某课外小组探究硫化钠晶体( Na2S·9H2O)在空气中放置后的氧化产物。取少量在空气中放置一段时间的硫化钠晶体样品,溶于水得到溶液A,测得溶液A的pH为13。
查阅资料:
i.硫化钠晶体在空气中放置后,可能会有Na2Sx、Na2SO3、Na2S2O3等物质生成。
ii.S2-、S 、S2O
、S2O 都不能使品红褪色,SO
都不能使品红褪色,SO 或高浓度OH- 能使品红褪色。
或高浓度OH- 能使品红褪色。
ii. Na2Sx能与H+反应生成H2S(臭鸡蛋气味气体)和S; Na2Sx能与Cu2+反应生成CuS (黑色固体)和S; Na2S2O3可与Cu2+形成可溶性络合物,该络合物对稀盐酸稳定,受热易分解生成棕黑色沉淀。
(1)取未在空气中放置的硫化钠晶体,溶于水后测得溶液显碱性,用离子方程式解释其原因为__________ 。
(2)进行实验一。
①实验一证明氧化产物中有Na2SO3, 其中编号2实验的目的是________________ 。
②某同学由实验结果进一步推测硫化钠晶体的氧化产物中可能还含有Na2SO4,这是因为Na2SO3有____ 性。
(3)进行实验二。
取溶液A于试管中,加入足量的稀盐酸,立即出现淡黄色浑浊,同时产生大量臭鸡蛋气味的气体,离心沉降(固液分离),得到无色溶液B和淡黄色固体。
①取无色溶液B______ (填操作和现象), 证明溶液A中存在SO 。
。
②该实验现象不能证明样品中存在Na2Sx,因为______________ 。
(4)进行实验三。

①证明氧化产物中存在Na2S2O3的证据是_______________ 。
②溶液A中加入CuCl2溶液生成黑色沉淀,可能发生的反应是______ (用离子方程式表示)。
结论:硫化钠晶体在空气中放置后的氧化产物有Na2SO3、Na24SO4、Na2Sx和Na2S2O3。
查阅资料:
i.硫化钠晶体在空气中放置后,可能会有Na2Sx、Na2SO3、Na2S2O3等物质生成。
ii.S2-、S
ii. Na2Sx能与H+反应生成H2S(臭鸡蛋气味气体)和S; Na2Sx能与Cu2+反应生成CuS (黑色固体)和S; Na2S2O3可与Cu2+形成可溶性络合物,该络合物对稀盐酸稳定,受热易分解生成棕黑色沉淀。
(1)取未在空气中放置的硫化钠晶体,溶于水后测得溶液显碱性,用离子方程式解释其原因为
(2)进行实验一。
 | 编号 | 试剂 | 现象 |
| 1 | 溶液A | 立即褪色 | |
| 2 | pH=13的NaOH溶液 | 无明显变化 |
②某同学由实验结果进一步推测硫化钠晶体的氧化产物中可能还含有Na2SO4,这是因为Na2SO3有
(3)进行实验二。
取溶液A于试管中,加入足量的稀盐酸,立即出现淡黄色浑浊,同时产生大量臭鸡蛋气味的气体,离心沉降(固液分离),得到无色溶液B和淡黄色固体。
①取无色溶液B
②该实验现象不能证明样品中存在Na2Sx,因为
(4)进行实验三。

①证明氧化产物中存在Na2S2O3的证据是
②溶液A中加入CuCl2溶液生成黑色沉淀,可能发生的反应是
结论:硫化钠晶体在空气中放置后的氧化产物有Na2SO3、Na24SO4、Na2Sx和Na2S2O3。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


