解答题-原理综合题 适中0.65 引用2 组卷168
在一定条件下,CO2可与H2发生反应生成甲醇,反应的化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。根据所学知识,回答下列问题:
CH3OH(g)+H2O(g)。根据所学知识,回答下列问题:
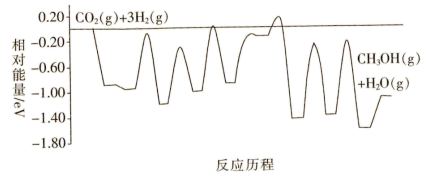
(1)CO2和H2在某催化剂表面合成甲醇的反应历程如图所示,由此判断CO2(g)+3H2(g) CH3OH(g)+H2O(g)是
CH3OH(g)+H2O(g)是___ (填“吸热”或“放热”)反应。
(2)若以CO2表示的该反应的化学反应速率为0.2mol•L-1•min-1,则以H2表示的该反应的化学反应速率为___ mol•L-1•min-1。
(3)恒温条件下,在2L的恒容密闭容器中,充入2molCO2和3molH2,在一定条件下发生反应。
①3s末测得CO2的物质的量为1.6mol,此时容器内CH3OH的物质的量浓度为___ mol•L-1,c(CO2):c(H2)=___ 。
②一段时间后,能说明该反应已达到平衡状态的是___ (填标号)。
a.c(CO2):c(H2O)
b.容器内压强保持不变
c.3v逆(CH3OH)=v正(H2)
d.容器内混合气体的密度保持不变
③若反应在ts后达到平衡,测得H2转化了50%,则平衡时CO2的体积分数为___ 。
④CH3OH是一种重要的化工产品。通过上述反应获得CH3OH是一种重要的途径,下列有关说法中正确的是___ (填标号)。
a.该反应为可逆反应,故在一定条件下CO2和H2不可能全部转化为CH3OH
b.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为0
c.在利用上述反应生产CH3OH时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
(1)CO2和H2在某催化剂表面合成甲醇的反应历程如图所示,由此判断CO2(g)+3H2(g)

(2)若以CO2表示的该反应的化学反应速率为0.2mol•L-1•min-1,则以H2表示的该反应的化学反应速率为
(3)恒温条件下,在2L的恒容密闭容器中,充入2molCO2和3molH2,在一定条件下发生反应。
①3s末测得CO2的物质的量为1.6mol,此时容器内CH3OH的物质的量浓度为
②一段时间后,能说明该反应已达到平衡状态的是
a.c(CO2):c(H2O)
b.容器内压强保持不变
c.3v逆(CH3OH)=v正(H2)
d.容器内混合气体的密度保持不变
③若反应在ts后达到平衡,测得H2转化了50%,则平衡时CO2的体积分数为
④CH3OH是一种重要的化工产品。通过上述反应获得CH3OH是一种重要的途径,下列有关说法中正确的是
a.该反应为可逆反应,故在一定条件下CO2和H2不可能全部转化为CH3OH
b.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为0
c.在利用上述反应生产CH3OH时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
20-21高一下·云南大理·阶段练习
类题推荐
甲烷和甲醇(CH3OH)既是重要的化工原料,又是未来重要的能源物质。
(1)通过CO(g)和H2(g)化合可制得甲醇。反应为 ,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量___________ (填“>”、“<”或“=”)1molCH3OH(g)的能量。 。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率v(CO)=
。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率v(CO)=___________ mol·L-1·min-1,V=___________ L;
(3)下列描述中能说明该反应已达平衡状态的是___________(填字母)。
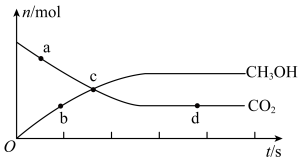
(4)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应: 。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:___________ (填“a”、“b”、“c”或“d”);用同一物质表示反应速率时,a、c两点的正反应速率:va___________ vc (填“>”、“<”或“=”,下同),该反应达到平衡时,CO2的转化率___________ 50%。
(1)通过CO(g)和H2(g)化合可制得甲醇。反应为

(3)下列描述中能说明该反应已达平衡状态的是___________(填字母)。
| A.断裂3mol H−H键时,生成2mol H−O键 |
| B.容器内混合气体的平均摩尔质量保持不变 |
| C.容器内混合气体的压强保持不变 |
| D.容器内CO与H2的体积之比保持不变 |
(4)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应:
工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
请回答下列问题:
(1)判断反应①是________ (填“吸热”或“放热”)反应
(2)据据反应①与反应②可推导出K1、K2与K3之间的关系,则K3 =________ (用K1、K2表示)
(3)某温度下反应①式中各物质的平衡浓度符合下式:20c(CH3OH) = 3c(CO)·c2(H2),试判断此时的温度为________ 。
(4)500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分别为0.4 mol·L-1、1 mol·L-1、0.5 mol·L-1、0.4 mol·L-1,则此时ν(正)________ ν(逆)(填“>”、“=”或“<”)。
(5)一定条件下将H2(g)和CO2(g)以体积比3:1置于恒温恒容的密闭容器发生反应③,下列能说明该反应达到平衡状态的有_____________
A.体系密度保持不变
B.H2和CO2的体积比保持不变
C.混合气体的平均相对分子量不变时,反应一定达到平衡状态
D.当破坏CO2中2个碳氧双键,同时破坏H2O 中的2个氧氢键,反应一定达到平衡状态
(6)若500℃时在2L密闭容器中加入2molH2和amolCO2进行②的反应,反应5min后达到平衡,平衡时CO2的转化率为50%,求a =________ mol,用H2表示该反应达到平衡时的平均反应速率ν(H2) =________ mol·L-1·min-1
化学反应 | 平衡常数 | 温度 | ||
500℃ | 700℃ | 800℃ | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) H2O(g)+CO(g) H2O(g)+CO(g) | K2 | 1 | 1.7 | 2.52 |
③3H2(g)+CO2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | K3 | |||
请回答下列问题:
(1)判断反应①是
(2)据据反应①与反应②可推导出K1、K2与K3之间的关系,则K3 =
(3)某温度下反应①式中各物质的平衡浓度符合下式:20c(CH3OH) = 3c(CO)·c2(H2),试判断此时的温度为
(4)500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分别为0.4 mol·L-1、1 mol·L-1、0.5 mol·L-1、0.4 mol·L-1,则此时ν(正)
(5)一定条件下将H2(g)和CO2(g)以体积比3:1置于恒温恒容的密闭容器发生反应③,下列能说明该反应达到平衡状态的有
A.体系密度保持不变
B.H2和CO2的体积比保持不变
C.混合气体的平均相对分子量不变时,反应一定达到平衡状态
D.当破坏CO2中2个碳氧双键,同时破坏H2O 中的2个氧氢键,反应一定达到平衡状态
(6)若500℃时在2L密闭容器中加入2molH2和amolCO2进行②的反应,反应5min后达到平衡,平衡时CO2的转化率为50%,求a =
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



