解答题-工业流程题 适中0.65 引用1 组卷151
铁在地壳中的含量很高,铁及其化合物也是人们日常生活中应用广泛的一类物质。请根据实验回答下列问题:
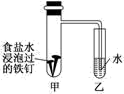
Ⅰ、将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中:
(1)发生的电化学腐蚀类型是___________ ,负极反应式为___________ 。
(2)过一段时间,乙试管中观察到的现象是___________
Ⅱ、实验室配置0.01mol•L﹣1FeCl2溶液时,需向溶液中滴加几滴稀盐酸,其目的是___________ ,还需要加入少量铁粉,其目的是___________ 。FeCl2溶液中离子浓度由大到小的顺序是___________ 。
Ⅲ、高铁酸盐是一种新型的净水剂,如高铁酸钾(K2FeO4),其净水过程中既表现出强氧化性,又表现了强吸附性,则K2FeO4与水反应的离子方程式为___________ 。
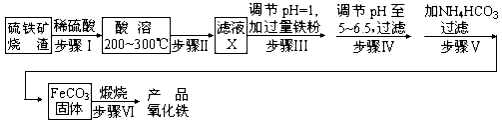
Ⅳ、工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)步骤1酸溶后的不溶物为___________ 。
(2)步骤Ⅳ中应选用___________ 试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是___________ 。
(4)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为9.5,c(Fe2+)=1×10—6mol/L。试判断所得的FeCO3中是否含有Fe(OH)2___________ (填“是”或“否”),请通过简单计算说明理由___________ (已知:Ksp[Fe(OH)2]=4.9×10—17)

Ⅰ、将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中:
(1)发生的电化学腐蚀类型是
(2)过一段时间,乙试管中观察到的现象是
Ⅱ、实验室配置0.01mol•L﹣1FeCl2溶液时,需向溶液中滴加几滴稀盐酸,其目的是
Ⅲ、高铁酸盐是一种新型的净水剂,如高铁酸钾(K2FeO4),其净水过程中既表现出强氧化性,又表现了强吸附性,则K2FeO4与水反应的离子方程式为
Ⅳ、工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)步骤1酸溶后的不溶物为
(2)步骤Ⅳ中应选用
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是
(4)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为9.5,c(Fe2+)=1×10—6mol/L。试判断所得的FeCO3中是否含有Fe(OH)2
19-20高二下·河南·期末
类题推荐
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料-----铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为_____________________________ ;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有___________ 、玻璃棒和烧杯等;步骤Ⅳ中应选用______ 试剂调节溶液的pH(填字母编号)
(3)检验步骤Ⅲ已经进行完全的试剂是________________ ;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是________________ ;
(5)步骤Ⅵ中发生反应的化学反应方程式为_____________________________ ;
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol•L-1.试判断所得的FeCO3中是否含有Fe(OH)2__________ (填“是”或“否”),请通过简单计算说明理由__________________________ (已知:Ksp[Fe(OH)2]=4.9×10-17)。

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有
| A.稀硝酸 | B.氢氧化钠溶液 | C.高锰酸钾溶液 | D.氨水 |
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是
(5)步骤Ⅵ中发生反应的化学反应方程式为
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6 mol•L-1.试判断所得的FeCO3中是否含有Fe(OH)2
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为______________________ ;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有_______________ 、玻璃棒和烧杯等;步骤Ⅳ中应选用_______________ 试剂调节溶液的pH(填字母编号)。
(3)检验步骤Ⅲ已经进行完全的试剂是____________________ ;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是___________________ ;
(5)步骤Ⅵ中发生反应的化学反应方程式为________________________ ;
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6mol·L-1。试判断所得的FeCO3中是否含有Fe(OH)2___________ (填“是”或“否”),请通过简单计算说明理由。
(已知:Ksp[Fe(OH)2]=4.9×10-17);
(7)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为____________ 。

试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有
| A.稀硝酸 | B.氢氧化钠溶液 | C.高锰酸钾溶液 | D.氨水 |
(3)检验步骤Ⅲ已经进行完全的试剂是
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是
(5)步骤Ⅵ中发生反应的化学反应方程式为
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10-6mol·L-1。试判断所得的FeCO3中是否含有Fe(OH)2
(已知:Ksp[Fe(OH)2]=4.9×10-17);
(7)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网