填空题 适中0.65 引用1 组卷292
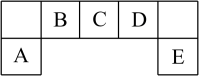
如图是元素周期表的一部分,主族元素A、B、C、D、E在元素周期表中的位置如图,A元素的单质在空气中含量最高(请用相应的元素符号或化学式作答)∶
(1)A简单离子结构示意图_______
(2)下列说法不正确的是_______
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为_______ ,A和D氢化物沸点的大小为_______ 。
(4)设计实验比较D与E的非金属性强(用离子方程式表示)_______ 。
(5)A2的结构式_____ ,CB4的电子式为____ ,CB4溶于NaOH溶液的化学方程式____ 。
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式_______ 。
| A | B | ||
| C | D | E |
(1)A简单离子结构示意图
(2)下列说法不正确的是
A.C的最高价氧化物能溶于B的氢化物水溶液
B.元素A、E的气态氢化物相遇会产生白烟
C.B元素形成的其中一种18电子分子,能与A元素形成的一种10电子分子发生氧化还原反应
D.原子得电子能力∶D>E>A
(3)C、D、B氢化物的稳定性大小为
(4)设计实验比较D与E的非金属性强(用离子方程式表示)
(5)A2的结构式
(6)E单质通入足量Na2CO3溶液发生反应的化学方程式
19-20高一下·四川成都·期中
类题推荐
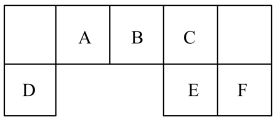
前四周期元素A、B、C、D、E、F、G、H的原子序数依次增大,在元素周期表中A的原子半径最小,B与C相邻且C的最外层电子数是次外层的3倍, 与
与 具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:
具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:
(1)C在元素周期表中的位置为___________ , 的离子结构示意图
的离子结构示意图___________ 。
(2)C和D也可形成一种漂白性物质,其电子式为___________ , 是
是___________ 键(填“极性键”或“非极性键”)构成的___________ 分子(填“极性”或“非极性”)。
(3)比较C和F简单氢化物的键角大小:___________ (用化学式表示),F和G的最高价氧化物的水化物酸性较强的是___________ (用化学式表示)。
(4)比较C、D、E三者离子半径的大小:___________ (用离子符号表示)。
(5)下列叙述正确且能用于比较元素D和E金属性强弱的是___________(填序号)。
(6)过量的 与G的单质的反应方程式:
与G的单质的反应方程式:___________ 。
(7)H的氢氧化物可溶于B的简单氢化物对应的水溶液反应,其离子方程式为___________ 。
(1)C在元素周期表中的位置为
(2)C和D也可形成一种漂白性物质,其电子式为
(3)比较C和F简单氢化物的键角大小:
(4)比较C、D、E三者离子半径的大小:
(5)下列叙述正确且能用于比较元素D和E金属性强弱的是___________(填序号)。
| A.在化合物中E的化合价比D的高 |
| B.E的单质不能与冷水反应而D的单质能 |
| C.E的最高价氧化物对应水化物的碱性比D弱 |
| D.D的单质无法从E的盐溶液中置换出E |
(7)H的氢氧化物可溶于B的简单氢化物对应的水溶液反应,其离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网