解答题-实验探究题 适中0.65 引用1 组卷170
浓硫酸有多种化学性质,如吸水性、脱水性、强氧化性、酸性等
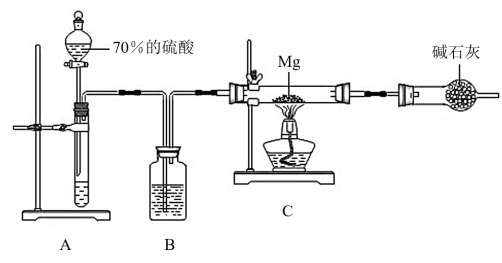
Ⅰ.甲同学用浓硫酸与木炭的反应探究浓硫酸的强氧化性。已知在加热条件下浓硫酸与木炭可发生化学反应,为了检验反应的产物,某同学用以下装置进行试验。请据此回答下列问题:
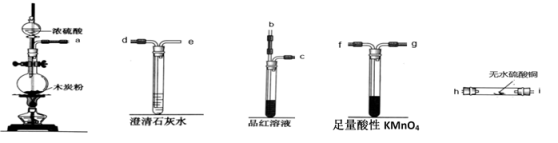
(1)如何检查木炭与浓硫酸反应装置的气密性?___________
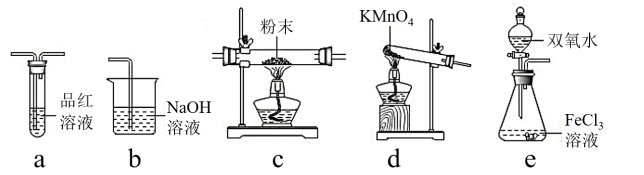
(2)为了完成实验,请将装置的接口按顺序连接(气流方向从左到右)a___________、___________、___________、___________fg___________;_________________
(3)实验过程中发现无水硫酸铜固体变为蓝色,品红溶液褪色,由此可知有水和SO2生成,利用氧化还原反应的规律推测还应该有CO2生成,证明有CO2气体生成的实验现象是___________
(4)依据上面的结论,写出木炭与浓硫酸反应的化学方程式___________
Ⅱ.乙同学用A制备SO2,并进一步制备抗氧化剂Na2S2O5,实验前已除尽装置内的空气。
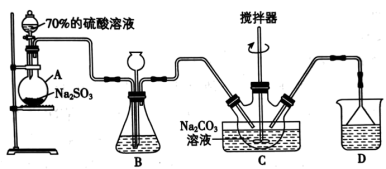
(5)制取二氧化硫选用70%浓硫酸,体现了硫酸的___________ 性
(6)装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用___________
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
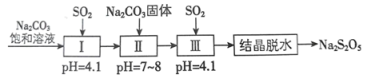
(7)焦亚硫酸钠(Na2S2O5)的制备。若步骤Ⅰ中通入足量的SO2,则该步骤反应的离子方程式为___________
Ⅰ.甲同学用浓硫酸与木炭的反应探究浓硫酸的强氧化性。已知在加热条件下浓硫酸与木炭可发生化学反应,为了检验反应的产物,某同学用以下装置进行试验。请据此回答下列问题:

(1)如何检查木炭与浓硫酸反应装置的气密性?
(2)为了完成实验,请将装置的接口按顺序连接(气流方向从左到右)a___________、___________、___________、___________fg___________;
(3)实验过程中发现无水硫酸铜固体变为蓝色,品红溶液褪色,由此可知有水和SO2生成,利用氧化还原反应的规律推测还应该有CO2生成,证明有CO2气体生成的实验现象是
(4)依据上面的结论,写出木炭与浓硫酸反应的化学方程式
Ⅱ.乙同学用A制备SO2,并进一步制备抗氧化剂Na2S2O5,实验前已除尽装置内的空气。

(5)制取二氧化硫选用70%浓硫酸,体现了硫酸的
(6)装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(7)焦亚硫酸钠(Na2S2O5)的制备。若步骤Ⅰ中通入足量的SO2,则该步骤反应的离子方程式为

20-21高一下·湖北·阶段练习
类题推荐
Ⅰ.某实验小组为探究含硫化合物(NH4)2S2O8的性质,设计如下实验探究(NH4)2S2O8的氧化性。
实验操作:向小试管中加入 溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量
溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量 溶液,试管中溶液立即变蓝,取上层清液检验,证明溶液中存在
溶液,试管中溶液立即变蓝,取上层清液检验,证明溶液中存在 ,回答下列问题
,回答下列问题
(1) 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(2)检验该溶液中存在 的具体操作及现象为
的具体操作及现象为_______ 。
(3)实验结论: 的氧化性
的氧化性_______ (填“强于”或“弱于”)I2。
已知:I2可与 发生反应:
发生反应: ,为了进一步探究
,为了进一步探究 与
与 的反应速率,小组同学设计下表实验:
的反应速率,小组同学设计下表实验:
(4)上述实验b中的
_______ ;
_______ 。
加入 溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
猜想1: 与
与 反应的速率远低于
反应的速率远低于 与
与 反应的速率;
反应的速率;
猜想2: 先与
先与 反应,
反应, 消耗完后才与
消耗完后才与 反应。
反应。
为验证上述猜想,小组同学补充下表实验:
(5)验证猜想1的实验设计为_______ (填“实验c”或“实验d”下同),验证猜想2的实验设计为_______ 。
(6)实验c中下层溶液显浅紫色的原因为_______ 。
(7)由上述实验可知_______ (填“猜想1”或“猜想2”)成立。
Ⅱ.Na2S2O5常用作纺织业棉麻脱氯剂;酸化时可放出SO2气体,其制备工艺流程
如下:
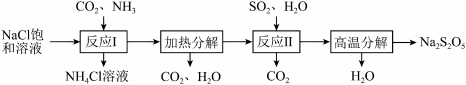
(8)Na2S2O5的名称为_______ (选填“焦硫酸钠”或“焦亚硫酸钠”)。
(9)“反应I ”中应先通入的气体是_______ ,反应后析出的固体产物是_______ 。
(10)“反应Ⅱ”的化学方程式为_______ 。
(11)若反应条件或用量等控制不当,则所得的Na2S2O5产品中往往含有杂质。
①若产品中含有杂质Na2SO3,其具体原因可能是_______ (任答一条即可)。
②若检验产品中含有杂质Na2CO3,下列试剂的使用顺序依次为_______ (填编号)。
a.稀硫酸 b.澄清石灰水 c.品红溶液 d.酸性KMnO4溶液
(12)Na2S2O3也可用作棉麻的脱氯剂。
①Na2S2O5溶液与Cl2反应的离子方程式为_______ 。
②Na2S2O5与Na2S2O3脱氯等效时,消耗二者的质量之比为_______ 。
实验操作:向小试管中加入
(1)
(2)检验该溶液中存在
(3)实验结论:
已知:I2可与
| 试验编号 | 蒸馏水/ | 0.4%的淀粉溶液/滴 | 变色时间/s | |||
| a | 4.0 | 0 | 4.0 | 2 | 2.0 | 立即 |
| b | 4.0 | 1.0 | 2 | 30 |
(4)上述实验b中的
加入
猜想1:
猜想2:
为验证上述猜想,小组同学补充下表实验:
| 试验编号 | 0.4%的淀粉溶液/滴 | 实验现象 | |||||
| c | 2 | 0 | 20 | 10 | 0 | 0.2 | 下层溶液显浅紫色 |
| d | 0 | 5 | 20 | 0 | 2 | 20 | 溶液先变蓝,后迅速褪色,一段时间后又变蓝 |
(5)验证猜想1的实验设计为
(6)实验c中下层溶液显浅紫色的原因为
(7)由上述实验可知
Ⅱ.Na2S2O5常用作纺织业棉麻脱氯剂;酸化时可放出SO2气体,其制备工艺流程
如下:

(8)Na2S2O5的名称为
(9)“反应I ”中应先通入的气体是
(10)“反应Ⅱ”的化学方程式为
(11)若反应条件或用量等控制不当,则所得的Na2S2O5产品中往往含有杂质。
①若产品中含有杂质Na2SO3,其具体原因可能是
②若检验产品中含有杂质Na2CO3,下列试剂的使用顺序依次为
a.稀硫酸 b.澄清石灰水 c.品红溶液 d.酸性KMnO4溶液
(12)Na2S2O3也可用作棉麻的脱氯剂。
①Na2S2O5溶液与Cl2反应的离子方程式为
②Na2S2O5与Na2S2O3脱氯等效时,消耗二者的质量之比为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网