单选题 适中0.65 引用3 组卷459
在两个锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入40mL1mol/L和40mL4mol/L的硫酸,装置如图。来比较以上两个反应的反应速率,下列说法正确的是
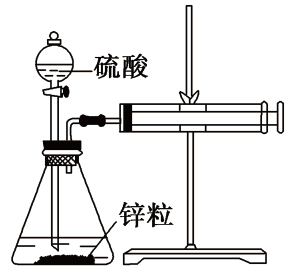

| A.锌粒和40mL1mol/L硫酸反应过程中,用Zn和H+表示该反应的反应速率的关系为v(Zn):v(H+)=1:2 |
| B.可以通过比较二者收集相同体积的H2所用的时间来比较两个反应的速率 |
| C.在相同条件下,1mol/L的硫酸与锌的反应速率更快 |
| D.该实验所需要的主要仪器就是以上装置中的仪器,不需要其它仪器 |
20-21高一下·湖北·阶段练习
类题推荐
某温度下按如图安装好实验装置,在锥形瓶内盛6.5 g锌粒(颗粒大小基本相同),通过分液漏斗加入40 mL 2.5 mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10 s时恰好收集到气体的体积为50 mL(若折合成0 ℃、101 kPa条件下的H2体积为44.8 mL),在该温度下,下列说法不正确的是( )
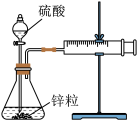

| A.用锌粒来表示10 s内该反应的速率为0.013 g/s |
| B.忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol/(L·s) |
| C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应的速率为0.01 mol/(L·s) |
| D.用H2来表示10 s内该反应的速率为0.000 2 mol/s |
某温度下按如图安装好实验装置,在锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液漏斗加入40mL2.5mol/L的稀硫酸溶液,将产生的H2收集在一个注射器中,0~10s内收集到气体的体积为50mL(折合成0℃、101kPa条件下的H2体积为44.8mL)。下列说法不正确的是
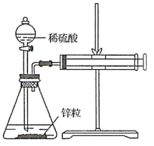

| A.将题述中的稀硫酸改为浓硫酸,生成H2的速率变快 |
| B.忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率为0.01 mol∙L−1∙s−1 |
| C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率为0.3mol∙L−1∙min−1 |
| D.可通过测定溶液的pH来测定反应速率 |
某温度下按如图安装好实验装置,在锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液漏斗加入40mL2.5mol/L的稀硫酸溶液,将产生的H2收集在一个注射器中,0~10s内收集到气体的体积为50mL(折合成0℃、101kPa条件下的H2体积为44.8mL)。下列说法不正确的是( )
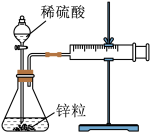

| A.将题述中的稀硫酸改为浓硫酸,生成H2的速率变快 |
| B.忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率为0.01mol/(L•s) |
| C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率为0.01mol/(L•s) |
| D.可通过测定溶液的pH来测定反应速率 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


