解答题-原理综合题 适中0.65 引用2 组卷501
国务院总理李克强在2021年国务院政府工作报告中指出,扎实做好碳达峰、碳中和各项工作,优化产业结构和能源结构,努力争取2060年前实现碳中和。碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)→CH2ClCHClCH3(g) ΔH=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)→CH2=CHCH2Cl(g)+HCl(g) ΔH=-100kJ·mol-1
①写出相同条件下CH2=CHCH2C1和HCl合成CH2ClCHClCH3的热化学方程式____ 。
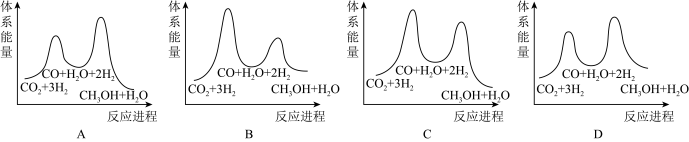
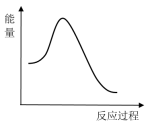
②已知①中的正反应的活化能E正为132kJ·mol-1,请在下图中标出①中逆反应的活化能E逆及数值_______ 。
(2)温度为T℃时向容积为2L的密闭容器中投入3molH2和1molCO2发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1,反应达到平衡时,测得放出热量19.76kJ,求平衡时:
①H2的转化率为_______
②T℃时该反应的平衡常数K=_______ (列计算式表示)。
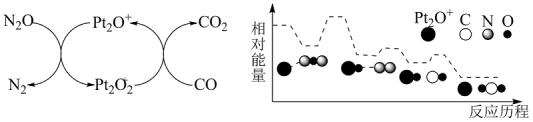
(3)目前有Ni-CeO2催化CO2加H2形成CH4的反应,历程如图所示,吸附在催化剂表面的物种用*标注。
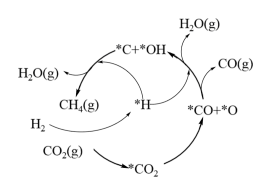
①写出上述转换中存在的主要反应的化学方程式_____ 。
②有人提出中间产物CO的处理,用反应2CO(g)=2C(s)+O2(g) ΔH>0来消除CO的污染,请用文字说明是否可行_____ 。
(4)T℃,HCOOH与CH3COONa溶液反应:HCOOH+CH3COO-⇌HCOO-+CH3COOH,该反应的K=12.5,则该温度下醋酸的电离常数Ka(CH3COOH)=_____ (T℃时Ka(HCOOH)=2×10-4)。
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)→CH2ClCHClCH3(g) ΔH=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)→CH2=CHCH2Cl(g)+HCl(g) ΔH=-100kJ·mol-1
①写出相同条件下CH2=CHCH2C1和HCl合成CH2ClCHClCH3的热化学方程式
②已知①中的正反应的活化能E正为132kJ·mol-1,请在下图中标出①中逆反应的活化能E逆及数值

(2)温度为T℃时向容积为2L的密闭容器中投入3molH2和1molCO2发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1,反应达到平衡时,测得放出热量19.76kJ,求平衡时:
①H2的转化率为
②T℃时该反应的平衡常数K=
(3)目前有Ni-CeO2催化CO2加H2形成CH4的反应,历程如图所示,吸附在催化剂表面的物种用*标注。

①写出上述转换中存在的主要反应的化学方程式
②有人提出中间产物CO的处理,用反应2CO(g)=2C(s)+O2(g) ΔH>0来消除CO的污染,请用文字说明是否可行
(4)T℃,HCOOH与CH3COONa溶液反应:HCOOH+CH3COO-⇌HCOO-+CH3COOH,该反应的K=12.5,则该温度下醋酸的电离常数Ka(CH3COOH)=
2021·天津北辰·一模
类题推荐
碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) △H1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2C1(g)+HCl(g) △H2=-100kJ·mol-1
在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g)的正反应活化能Ea(正)为132kJ·mol-1,则逆反应的活化能Ea(逆)为_______ kJ·mol-1
(2)在一定条件下可发生分解反应:CH3CHO(g)=CH4(g)+CO(g)某温度下向恒容密闭容器中加入一定量CH3CHO,测得CH3CHO浓度随时间的变化如表所示:
①2~5min内用CH3CHO表示的该反应的平均反应速率为_______ 。
②一定温度下,在恒容密闭容器中充入一定量CH3CHO进行该反应,能判断反应已达到化学平衡状态的是_______ 。
A.CH4和CO的浓度比保持不变
B.容器中压强不再变化
C.4molC-H断裂同时1molC≡O生成
D.气体的密度保持不变
(3)在一密闭容器中,起始时向该容器中充入6molH2S和3molCH4,发生反应:CH4(g)+2H2S(g) CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
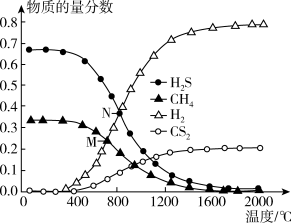
①该反应的△H_______ 0(填“>”或“<”)
②为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_______ (列举一条)。N点对应温度下,该反应的Kp=_______ (MPa)2(Kp为以分压表示的平衡常数)。
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) △H1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2C1(g)+HCl(g) △H2=-100kJ·mol-1
在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g)的正反应活化能Ea(正)为132kJ·mol-1,则逆反应的活化能Ea(逆)为
(2)在一定条件下可发生分解反应:CH3CHO(g)=CH4(g)+CO(g)某温度下向恒容密闭容器中加入一定量CH3CHO,测得CH3CHO浓度随时间的变化如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量CH3CHO进行该反应,能判断反应已达到化学平衡状态的是
A.CH4和CO的浓度比保持不变
B.容器中压强不再变化
C.4molC-H断裂同时1molC≡O生成
D.气体的密度保持不变
(3)在一密闭容器中,起始时向该容器中充入6molH2S和3molCH4,发生反应:CH4(g)+2H2S(g)

①该反应的△H
②为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网