单选题 适中0.65 引用2 组卷248
二氧化硫是一种应用广泛的化工原料。在接触法制硫酸的工业中,二氧化硫制取三氧化硫的反应为2SO2(g)+O2(g) = 2SO3(g) ∆H= -196 kJ•mol-1.实验室用亚硫酸钠固体与70%的硫酸制取少量的二氧化硫。下列有关用二氧化硫制取三氧化硫的说法正确的是
| A.反应的∆S > 0 |
| B.2 mol SO2与足量O2反应,放出的热量为196 kJ |
| C.工业上用通入足量的空气来提高SO2的转化率 |
| D.反应中每消耗1 mol SO2转移的电子数目约等于4×6.02×1023 |
20-21高二下·江苏无锡·阶段练习
类题推荐
二氧化硫是一种重要的化工原料,可以制取硫酸、焦亚硫酸钠等化工产品。其中,催化制取三氧化硫的热化学方程式为: △H=-196.6 kJ·mol
△H=-196.6 kJ·mol 。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是
。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是
| A.该反应中,反应物的键能之和<产物的键能之和 |
| B.反应中每充入2 mol SO2和1 mol O2,充分反应后转移电子数目为 |
| C.使用优质催化剂,体系中 |
| D.升高温度,能加快反应速率,提高二氧化硫的平衡转化率 |
SO2是一种重要的化工原料,主要用于生产三氧化硫、亚硫酸盐等,生产SO3的反应为2SO2(g)+O2(g)⇌2SO3(g)∆H=-198KJ·mol-1。实验室用浓硫酸和Na2SO3固体反应制取少量SO2,SO2排放到大气中会形成酸雨。工业合成三氧化硫的的反应过程可用下图模拟( 代表O2分子,
代表O2分子, 代表SO2分子,
代表SO2分子,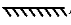 代表催化剂)。下列说法正确的是
代表催化剂)。下列说法正确的是

 代表O2分子,
代表O2分子, 代表SO2分子,
代表SO2分子,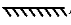 代表催化剂)。下列说法正确的是
代表催化剂)。下列说法正确的是
| A.过程Ⅰ和过程Ⅳ决定了整个反应进行的程度 |
| B.过程Ⅱ为放热反应,过程Ⅲ为吸热反应 |
| C.1 mol SO2和1 molO2反应,放出的热量小于99 kJ |
| D.催化剂可降低整个反应的活化能,因此使 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


