单选题 适中0.65 引用6 组卷887
一定温度下,难溶电解质在水中存在沉淀溶解和生成的平衡,常用溶度积Ksp来表示溶解程度的大小,如Ksp(AgCl)=c(Ag+)·c(Cl—)。常温下用0.1000mol/L的AgNO3标准溶液(pH≈5)分别滴定20.00mL0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg[定义为pAg=—lgc(Ag+)]与AgNO3溶液体积的变化关系如图所示。
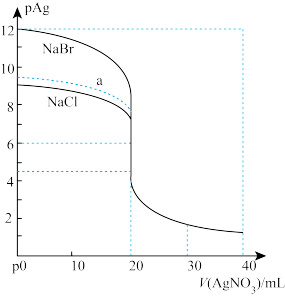
下列说法不正确的是

下列说法不正确的是
| A.Ksp(AgCl)>Ksp(AgBr) |
| B.当V(AgNO3溶液)=20mL时,NaBr溶液中:c(Ag+)+c(H+)=c(Br—)+c(OH—) |
| C.当V(AgNO3溶液)=30mL时,NaCl溶液中:c(NO |
| D.相同实验条件下,若改用10.00mL0.2000mol/LNaCl溶液,则滴定曲线(滴定终点前)可能变为a |
2021·浙江·三模
类题推荐
某温度下,分别向10.00 mL 0.1 mol·L-1 NaCl和Na2CrO4溶液中滴加0.1 mol·L-1 AgNO3溶液,滴加过程中-lgc(M)(M为Cl-或CrO )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
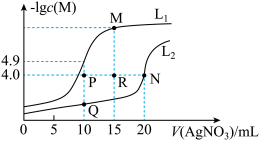

| A.该温度下,Ksp(Ag2CrO4) = 2×10-8 |
| B.该温度下,向浓度相同的 NaCl和Na2CrO4混合溶液滴加AgNO3溶液,先有粉红色沉淀生成 |
| C.M点溶液中:c(Na+)>c(NO |
| D.相同实验条件下,若改为 0.05 mol/L NaCl和Na2CrO4溶液,则曲线L2中N点移到P点 |
常温下,用0.1000mol/L的AgNO3标准溶液分别滴定20.00mL0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg与滴定百分数的变化关系如图所示。已知:pAg=-lgc(Ag+),滴定百分数指滴定所用标准溶液体积相对于滴定终点时所用标准溶液体积的百分数。下列说法不正确的是


| A.Ksp(AgCl)=1×10−9.5 |
| B.滴定百分数为50%时,NaCl溶液中:c(Na+)>c( |
| C.滴定百分数为100%时,NaCl溶液中:c(Ag+)+c(H+)=c(Cl−)+c(OH−) |
| D.滴定百分数为150%时,NaBr溶液中:c( |
体积和浓度均为25.00mL0.1mol/LNaI、NaBr及NaCl三种溶液,分别用0.1mol/L的AgNO3溶液滴定,滴定曲线如图所示[pAg=-lgc(Ag+)]。下列说法不正确的是


| A.Ksp(AgI)<Ksp(AgBr)<Ksp(AgCl) |
| B.AgNO3溶液滴定Cl-时,可加入少量的KI作滴定指示剂 |
| C.三种溶液等体积等浓度混合后用AgNO3溶液滴定,沉淀顺序为I-、Br-、Cl- |
| D.当V(AgNO3)=30.00mL时,三种溶液中:c(I-)<c(Br-)<c(Cl-) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


