解答题-工业流程题 适中0.65 引用1 组卷112
以镍废渣(主要成分为Ni,含少量Fe、Al、Fe3O4、Al2O3和不溶性杂质等)为原料获得碳酸镍流程如图:回答下列问题:[溶液中某离子浓度c(X)T≤10-5 mol·L-1时,即视为沉淀完全] 。
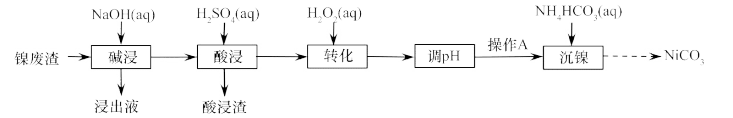
(1)“碱浸”时加入NaOH溶液的作用是___________ 。
(2)“酸浸”滤液中含有的阳离子主要为H+、___________ 。
(3)“转化”时加入H2O2的目的是___________ (用离子方程式表示),该过程温度不宜过高,原因可能是___________ 。
(4)请写出“沉镍”时的离子方程式___________ 。
(5)若选用Na2CO3溶液“沉镍”,当溶液中碳总浓度[ c(C)]为0.1 mol·L-1时,溶液中镍总浓度的对数[lgc(Ni)]与溶液pH关系如图。注:c(C)=c( )+c(
)+c( )+c(H2CO3)
)+c(H2CO3)

①a点(pH≈8.2)时溶液中析出的沉淀主要为___________ (填化学式)。
②b点溶液中Ni2+是否沉淀完全___________ (填“是”或“否”)
(6)取“操作A”所得的NiSO4溶液VmL,用c mol·L-1 EDTA(Na2H2Y)的标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+),消耗标准液20.00 mL,则“沉镍”过程中,当NiCO3开始沉淀时,溶液中 浓度为
浓度为___________ 。[已知常温下,Ksp(NiCO3)=1.42×10-7,只列计算式,不考虑杂质反应]。
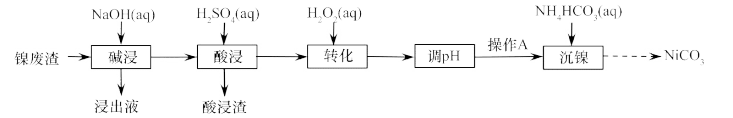
(1)“碱浸”时加入NaOH溶液的作用是
(2)“酸浸”滤液中含有的阳离子主要为H+、
(3)“转化”时加入H2O2的目的是
(4)请写出“沉镍”时的离子方程式
(5)若选用Na2CO3溶液“沉镍”,当溶液中碳总浓度[ c(C)]为0.1 mol·L-1时,溶液中镍总浓度的对数[lgc(Ni)]与溶液pH关系如图。注:c(C)=c(

①a点(pH≈8.2)时溶液中析出的沉淀主要为
②b点溶液中Ni2+是否沉淀完全
(6)取“操作A”所得的NiSO4溶液VmL,用c mol·L-1 EDTA(Na2H2Y)的标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+),消耗标准液20.00 mL,则“沉镍”过程中,当NiCO3开始沉淀时,溶液中
20-21高二下·四川广安·期中
类题推荐
某化工厂“用含NiO的废料(杂质为Fe2O3、 CaO、 CuO等)制备羟基氧化镍(2NiOOH·H2O)的工艺流程如图:
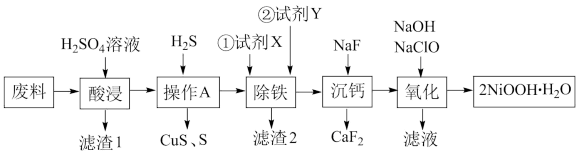
已知:相关金属离子形成氢氧化物沉淀的pH范围如图:
请回答下列问题:
(1)①滤渣1的主要成分是___________ 。
②如图是酸浸时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是___________ ℃,若酸浸时将温度控制在80℃左右,则滤渣1中会含有一定量的Ni(OH)2,其原因可能是___________ 。

(2)操作A中生成S的反应的离子方程式为:___________ 。
(3)试剂Y用于调节溶液的pH,则调控pH的范围是___________ 。
(4)写出沉钙后氧化过程中反应的离子方程式___________ 。
(5)沉钙时,当溶液中c(F-)=3.0×10-2 mol/L时,通过计算确定溶液中Ca2+是否沉淀完全___________ [已知:当离子浓度≤1.0×10-5时,认为该离子沉淀完全;常温时,Ksp(CaF2)=2.7×10-11]。

已知:相关金属离子形成氢氧化物沉淀的pH范围如图:
| 离子 | Fe3+ | Fe2+ | Ni2+ |
| 开始沉淀的pH | 2.7 | 7.6 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.6 | 9.2 |
请回答下列问题:
(1)①滤渣1的主要成分是
②如图是酸浸时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是

(2)操作A中生成S的反应的离子方程式为:
(3)试剂Y用于调节溶液的pH,则调控pH的范围是
(4)写出沉钙后氧化过程中反应的离子方程式
(5)沉钙时,当溶液中c(F-)=3.0×10-2 mol/L时,通过计算确定溶液中Ca2+是否沉淀完全
常温下,用含钴废料(主要成分为CoCO3,还含有少量NiCO3与铁屑)制备CoCl2•6H2O的工艺流程如图。
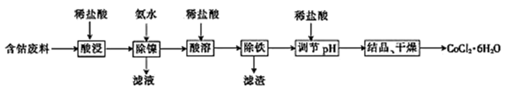
①已知除镍过程中溶液pH对钴的回收率及Ni2+含量的影响如图所示。
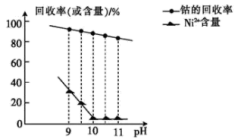
②部分金属阳离子在实验条件下开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)酸浸后溶液中的阳离子为:Co2+,Ni2+和__ 。
(2)除镍时,应调节溶液pH=__ ,此时Ni2+是否形成Ni(OH)2沉淀?___ (是或否)。若pH过小,则产品纯度会___ (升高,降低,或不变)。
(3)酸溶时,当调节pH=8时,溶液中n(Fe3+):n(Co2+)=__ 。
已知Ksp[Co(OH)2]=2.0×10-16,Ksp[Fe(OH)3]=4.0×10-38。
(4)除铁时先向溶液中加入30%的H2O2发生的离子反应方程式是:__ 。充分反应后再向溶液中加入CoCO3,调节溶液pH范围为__ ,使Fe3+完全转化为Fe(OH)3沉淀,最后过滤得到CoCl2溶液。
(5)已知Ag++SCN-=AgSCN↓,为测定粗产品中CoCl2•6H2O的含量,称取11.9g粗产品配成100mL溶液,从中取出25mL先加入含0.03mol的AgNO3,(杂质不与其反应),再用0.5mol/L的KSCN溶液标定过量的AgNO3,该标定操作所用的指示剂为__ (填化学式),若消耗20.00mL的KSCN溶液,则该粗产品中CoCl2•6H2O的质量分数为__ 。

①已知除镍过程中溶液pH对钴的回收率及Ni2+含量的影响如图所示。

②部分金属阳离子在实验条件下开始沉淀和完全沉淀的pH如表所示:
| 金属阳离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 1.5 | 4.0 |
| Fe2+ | 7.5 | 9.7 |
| Co2+ | 6.6 | 9.4 |
| Ni2+ | 7.7 | 9.5 |
回答下列问题:
(1)酸浸后溶液中的阳离子为:Co2+,Ni2+和
(2)除镍时,应调节溶液pH=
(3)酸溶时,当调节pH=8时,溶液中n(Fe3+):n(Co2+)=
已知Ksp[Co(OH)2]=2.0×10-16,Ksp[Fe(OH)3]=4.0×10-38。
(4)除铁时先向溶液中加入30%的H2O2发生的离子反应方程式是:
(5)已知Ag++SCN-=AgSCN↓,为测定粗产品中CoCl2•6H2O的含量,称取11.9g粗产品配成100mL溶液,从中取出25mL先加入含0.03mol的AgNO3,(杂质不与其反应),再用0.5mol/L的KSCN溶液标定过量的AgNO3,该标定操作所用的指示剂为
“翠矾”(NiSO4·7H2O)在印染工业作媒染剂,生产酞菁艳蓝络合剂;氟镍化钾(K2NiF4)是结构化学研究的热点物质。以镍废渣(主要成分为Ni,含少量Fe、Al、Fe3O4、Al2O3和不溶性杂质等)为原料合成“翠矾”和氟镍化钾的流程如下:
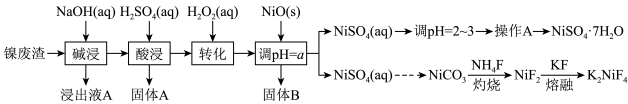
几种金属离子的氢氧化物沉淀pH如下:
请回答下列问题:
(1)翠矾、绿矾、明矾、蓝矾等“矾类”都含有______ 元素(填元素符号)。pH=a的范围为___________ 。
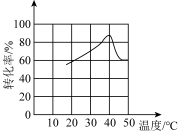
(2)“转化”过程中一定体积和浓度的双氧水,“转化率”与温度关系如图1所示。温度高于40℃,转化率急速降低的原因可能是______ 。空气可以替代双氧水,空气的作用是______ (用离子方程式表示)。
(3)NiSO4和NH4HCO3溶液生成NiCO3,其离子方程式为___________ 。
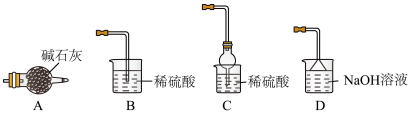
(4)灼烧NiCO3和NH4F以物质的量之比为1:1组成的混合物时,为避免污染环境,选择下列装置吸收尾气,最宜选择___________ 。(填选项)
(5)已知常温下,Ksp(NiCO3)=1.42×10-7。分离NiCO3时滤液中c(Ni2+)≤1.0×10-5 mol·L-1时,c(CO )≥
)≥___________ mol·L-1。
(6)准确称取ω g翠矾晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250 mL溶液,取20.00 mL所配溶液于锥形瓶,用c mol·L-1的标准溶液EDTA(Na2H2Y)滴定至终点(发生Ni2++H2Y2-=NiY2-+2H+),三次实验消耗标准液的体积分别为20.02 mL、19.98 mL、19.50 mL,则翠矾的纯度为___________ %(只列计算式,不考虑杂质反应)。

几种金属离子的氢氧化物沉淀pH如下:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.8 | 5.2 |
Fe2+ | 7.6 | 9.7 |
Ni2+ | 7.1 | 9.2 |

请回答下列问题:
(1)翠矾、绿矾、明矾、蓝矾等“矾类”都含有
(2)“转化”过程中一定体积和浓度的双氧水,“转化率”与温度关系如图1所示。温度高于40℃,转化率急速降低的原因可能是
(3)NiSO4和NH4HCO3溶液生成NiCO3,其离子方程式为
(4)灼烧NiCO3和NH4F以物质的量之比为1:1组成的混合物时,为避免污染环境,选择下列装置吸收尾气,最宜选择

(5)已知常温下,Ksp(NiCO3)=1.42×10-7。分离NiCO3时滤液中c(Ni2+)≤1.0×10-5 mol·L-1时,c(CO
(6)准确称取ω g翠矾晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250 mL溶液,取20.00 mL所配溶液于锥形瓶,用c mol·L-1的标准溶液EDTA(Na2H2Y)滴定至终点(发生Ni2++H2Y2-=NiY2-+2H+),三次实验消耗标准液的体积分别为20.02 mL、19.98 mL、19.50 mL,则翠矾的纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


