解答题-原理综合题 适中0.65 引用1 组卷314
苯乙烯是一种重要的化工原料,可采用乙苯催化脱氢法制备,反应原理如下:
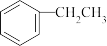 (g)⇌
(g)⇌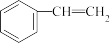 (g)+H2(g) ∆H
(g)+H2(g) ∆H
(1)已知:
计算上述反应的∆H=_____ 。
(2)生产过程中,在600℃时向乙苯中掺入高温水蒸气,保持体系总压为105.6kPa催化反应。若投料比n(乙苯)/n(H2O)=1:8,达平衡时乙苯的转化率为60%,则p(H2O)=____ kPa,平衡常数Kp=____ (Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)。若其他条件不变,将上述起始反应物置于某恒容密闭容器中,则乙苯的平衡转化率___ (填“>”“<”或“=”)60%。
(3)利用膜反应新技术,可以实现边反应边分离出生成的氢气。不同温度下,1.00mol乙苯在容积为1.00L的密闭容器中反应,氢气移出率α与乙苯平衡转化率关系如图所示:(氢气移出率 )
)
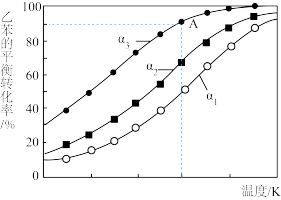
①同温度时α1、α2、α3依次____ (填“增大”或“减小”),理由是____ 。
②A点平衡常数 ,则α为
,则α为___ 。
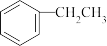 (g)⇌
(g)⇌ (g)+H2(g) ∆H
(g)+H2(g) ∆H(1)已知:
| 化学键 | C—H | C—C | C=C | H—H |
| 键能 | 412 | 348 | 612 | 436 |
(2)生产过程中,在600℃时向乙苯中掺入高温水蒸气,保持体系总压为105.6kPa催化反应。若投料比n(乙苯)/n(H2O)=1:8,达平衡时乙苯的转化率为60%,则p(H2O)=
(3)利用膜反应新技术,可以实现边反应边分离出生成的氢气。不同温度下,1.00mol乙苯在容积为1.00L的密闭容器中反应,氢气移出率α与乙苯平衡转化率关系如图所示:(氢气移出率

①同温度时α1、α2、α3依次
②A点平衡常数
2021·山东烟台·三模
类题推荐
工业上常采用乙苯催化脱氢制苯乙烯,方程式为: (g)
(g)
 (g)+H2(g)
(g)+H2(g)
(1)已知:
计算上述反应的△H=_____ kJ•mol﹣1。
(2)①利用计算结果与反应特点,选择理论上有利于提高苯乙烯平衡产率的条件_____ 。
A.低温B.高温C.高压D.低压E.合适的催化剂
②实际工业生产中常伴有乙苯裂解等副反应。而乙苯裂解反应无论在热力学还是在动力学上都比乙苯脱氢更有利,所以工业生产要使反应向脱氢方向进行需要采用_____ 条件来提高反应的选择性。
③工业生产中常采用恒压条件下向乙苯蒸汽中掺入水蒸气或CO2的办法来提高乙苯的平衡转化率,请从平衡移动的角度加以说明_____ 。
(3)利用膜反应新技术,可以实现边反应边分离出生成的氢气不同温度下,1.00mol乙苯在容积为1.00L的密闭容器中反应,氢气移出率α与乙苯平衡转化率关系如图所示:
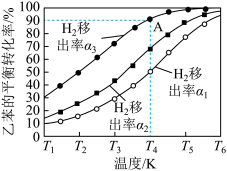
氢气移出率α
①同温度时α1、α2、α3依次_____ ,(填“增大”“减小”)原因是_____ 。
②A点平衡常数为0.45mol/L,则α为_____ 。
 (g)
(g) (g)+H2(g)
(g)+H2(g)(1)已知:
| 化学键 | C﹣H | C﹣C | C=C | H﹣H |
| 键能/kJ•mol﹣1 | 412 | 348 | 612 | 436 |
计算上述反应的△H=
(2)①利用计算结果与反应特点,选择理论上有利于提高苯乙烯平衡产率的条件
A.低温B.高温C.高压D.低压E.合适的催化剂
②实际工业生产中常伴有乙苯裂解等副反应。而乙苯裂解反应无论在热力学还是在动力学上都比乙苯脱氢更有利,所以工业生产要使反应向脱氢方向进行需要采用
③工业生产中常采用恒压条件下向乙苯蒸汽中掺入水蒸气或CO2的办法来提高乙苯的平衡转化率,请从平衡移动的角度加以说明
(3)利用膜反应新技术,可以实现边反应边分离出生成的氢气不同温度下,1.00mol乙苯在容积为1.00L的密闭容器中反应,氢气移出率α与乙苯平衡转化率关系如图所示:

氢气移出率α
①同温度时α1、α2、α3依次
②A点平衡常数为0.45mol/L,则α为
苯乙烯是一种重要的化工原判,可采用乙苯催化脱氢法制备,反应如下:
 (g)
(g)
 (g)+H2(g)△H
(g)+H2(g)△H
(1)已知
计算上述反应的△H=___ 。
(2)实际生产中往刚性容器中同时通入乙苯和大量水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。测得体系总压和乙苯转化率随时间变化结果如图所示。
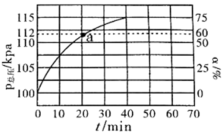
①请用化学平衡理论解释通入大量水蒸气的原因___ 。
②平衡时,p(H2O)=__ kPa,平衡常数Kp=__ kPa(Kp为以分压表示的平衡常数,气体分压=气体总压×体积分数)
③反应速率v=v正-v逆=k正·p(乙苯)-k逆·p(苯乙烯)·p(氢气),k正、k逆分别为正、逆反应速率常数。计算a处的 =
=___ 。
(3)苯乙烯与溴化氢发生的加成反应产物有两种,其反应的化学方程式如下:
i.C6H5-CH=CH2(g)+HBr(g) C6H5-CH2CH2Br(g)
C6H5-CH2CH2Br(g)
ii.C6H5-CH=CH2(g)+HBr(g) C6H5-CHBrCH3(g)
C6H5-CHBrCH3(g)
600℃时,向3L恒容密闭容器中充入1.2molC6H5-CH=CH2(g)和1.2molHBr(g)发生反应,达到平衡时C6H5-CH2CH2Br(g)和C6H5-CHBrCH3(g)的物质的量(n)随时间(t)变化的曲线如图所示。
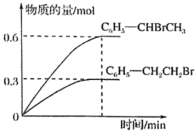
①600℃时,反应ii的化学平衡常数Kii=___ 。
②反应平衡后,若保持其他条件不变,向该容器中再充入1molC6H5-CH2CH2Br(g),则反应ii将__ (填“正向”“逆向”或“不”)移动。
③在恒温恒容的密闭容器中,苯乙烯与溴化氢发生i、ii两个加成反应,可以判断反应已达到平衡状态的是__ (填编号)。
A.容器内混合气体的密度不再改变
B.C6H5-CH2CH2Br(g)的生成速率与C6H5-CHBrCH3(g)的分解速率相等
C.反应器中压强不再随时间变化而变化
D.混合气体的平均相对分子质量保持不变
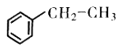 (g)
(g) (g)+H2(g)△H
(g)+H2(g)△H(1)已知
| 化学键 | C—H | C—C | C=C | H—H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
(2)实际生产中往刚性容器中同时通入乙苯和大量水蒸气,控制反应温度为600℃、体系起始总压强为100kPa的条件下进行反应。测得体系总压和乙苯转化率随时间变化结果如图所示。

①请用化学平衡理论解释通入大量水蒸气的原因
②平衡时,p(H2O)=
③反应速率v=v正-v逆=k正·p(乙苯)-k逆·p(苯乙烯)·p(氢气),k正、k逆分别为正、逆反应速率常数。计算a处的
(3)苯乙烯与溴化氢发生的加成反应产物有两种,其反应的化学方程式如下:
i.C6H5-CH=CH2(g)+HBr(g)
ii.C6H5-CH=CH2(g)+HBr(g)
600℃时,向3L恒容密闭容器中充入1.2molC6H5-CH=CH2(g)和1.2molHBr(g)发生反应,达到平衡时C6H5-CH2CH2Br(g)和C6H5-CHBrCH3(g)的物质的量(n)随时间(t)变化的曲线如图所示。

①600℃时,反应ii的化学平衡常数Kii=
②反应平衡后,若保持其他条件不变,向该容器中再充入1molC6H5-CH2CH2Br(g),则反应ii将
③在恒温恒容的密闭容器中,苯乙烯与溴化氢发生i、ii两个加成反应,可以判断反应已达到平衡状态的是
A.容器内混合气体的密度不再改变
B.C6H5-CH2CH2Br(g)的生成速率与C6H5-CHBrCH3(g)的分解速率相等
C.反应器中压强不再随时间变化而变化
D.混合气体的平均相对分子质量保持不变
国内外目前生产苯乙烯的方法主要是乙苯脱氢法,反应原理如下:
 (g)
(g)
 (g)+H2(g) ∆H1。
(g)+H2(g) ∆H1。
(1)已知:部分化学键的键能数据如下表所示:
则∆H1=_______
(2)实际生产过程中,通常向乙苯中掺入水蒸气,保持体系总压为常压(101kPa)的条件下进行反应。乙苯的平衡转化率与温度、投料比m[m= ]的关系如图1所示。
]的关系如图1所示。

①掺入水蒸气的目的是_______ ;
②投料比(m1、m2、m3)由大到小的顺序为________ ;
③若投料比m=1:9,反应温度为600℃,并保持体系总压为常压的条件下进行反应,下列事实不能作为该反应达到平衡的依据的是_______ (填选项字母)。
a.V正(乙苯)=v逆(乙苯)
b.容器内气体密度不再变化
c.容器内气体的平均相对分子质量不再变化
d.苯乙烯的体积分数不再变化。
e.容器内苯乙烯与H2的物质的量之比不再变化
④若m2=1:9,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数Kp=____ kPa(列出计算式即可,Kp为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数);若其他条件不变,将A点对应起始反应物置于某恒容密闭容器中,则乙苯的平衡转化率____ (填“>”“<”或“=”)60%。
(3)实验测得,乙苯脱氢反应的速率方程为v正=k正∙P乙苯,v逆=k逆∙P苯乙醚∙P氢气(k正、k逆为速率常数)。如图2(lgk表示速率常数的对数; 表示表示温度的倒数)所示,①②③④四条斜线中,lgk逆随
表示表示温度的倒数)所示,①②③④四条斜线中,lgk逆随 变化关系的是斜线③,则lgk正随
变化关系的是斜线③,则lgk正随 变化关系的是斜线
变化关系的是斜线_______ 。

(4)近年来,用CO2作为温和氧化剂,选择性氧化乙苯制苯乙烯的绿色反应体系不断取得新进展。在CO2气氛下,乙苯脱氢反应可能存在一步法和二步法两种途径,如图3所示。

则CO2(g)+ (g)
(g)
 (g)+CO(g)+H2O(g)反应的平衡常数K=
(g)+CO(g)+H2O(g)反应的平衡常数K=_____ (用含K1、K2的代数式表示)。
 (g)
(g) (g)+H2(g) ∆H1。
(g)+H2(g) ∆H1。(1)已知:部分化学键的键能数据如下表所示:
| 共价键 | C-C | C-H | C=C | H-H |
| 键能/(kJ∙mol-1) | 347.7 | 413.4 | 615 | 436 |
(2)实际生产过程中,通常向乙苯中掺入水蒸气,保持体系总压为常压(101kPa)的条件下进行反应。乙苯的平衡转化率与温度、投料比m[m=

①掺入水蒸气的目的是
②投料比(m1、m2、m3)由大到小的顺序为
③若投料比m=1:9,反应温度为600℃,并保持体系总压为常压的条件下进行反应,下列事实不能作为该反应达到平衡的依据的是
a.V正(乙苯)=v逆(乙苯)
b.容器内气体密度不再变化
c.容器内气体的平均相对分子质量不再变化
d.苯乙烯的体积分数不再变化。
e.容器内苯乙烯与H2的物质的量之比不再变化
④若m2=1:9,保持体系总压为常压(101kPa),则A点温度下,该反应的平衡常数Kp=
(3)实验测得,乙苯脱氢反应的速率方程为v正=k正∙P乙苯,v逆=k逆∙P苯乙醚∙P氢气(k正、k逆为速率常数)。如图2(lgk表示速率常数的对数;

(4)近年来,用CO2作为温和氧化剂,选择性氧化乙苯制苯乙烯的绿色反应体系不断取得新进展。在CO2气氛下,乙苯脱氢反应可能存在一步法和二步法两种途径,如图3所示。

则CO2(g)+
 (g)
(g) (g)+CO(g)+H2O(g)反应的平衡常数K=
(g)+CO(g)+H2O(g)反应的平衡常数K=组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


