解答题-实验探究题 适中0.65 引用2 组卷323
葡萄糖酸钙是一种常用的药物,临床上用于治疗骨质疏松症。某实验室对葡萄糖酸钙的制备工艺进行研究,先以葡萄糖[CH2OH(CHOH)4CHO]和H2O2为原料制备葡萄糖酸[CH2OH(CHOH)4COOH],再用葡萄糖酸与碳酸钙反应制备葡萄糖酸钙。已知:30%H2O2溶液的密度为1.1g·cm-3,回答下列问题:
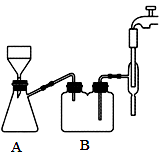
I.制备葡萄糖酸(装置如图所示)。
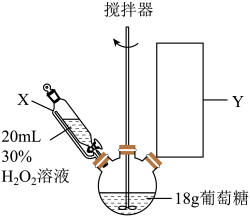
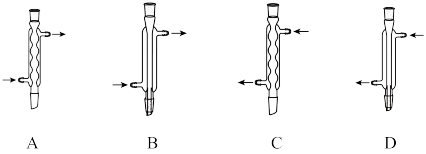
(1)仪器X的名称为___________ ,Y处为冷凝回流装置,下列仪器使用正确且效果最好的是___________ (填字母)。
(2)滴入双氧水,水浴加热一段时间后,得到无色透明的葡萄糖酸溶液。反应的化学方程式为___________ 。
Ⅱ.测定葡萄糖的转化率,确定合适的反应温度。
(3)用移液管取出三口烧瓶中的反应液2.00mL置于锥形瓶中,以酚酞作为指示剂并加20mL蒸馏水稀释,用0.04mol·L-1NaOH标准溶液滴定。
①滴定管使用的正确的操作顺序为蒸馏水洗涤→标准液润洗→___________ →___________ →___________ →___________ →洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②达到滴定终点时的现象为___________ 。
③滴定过程消耗NaOH标准溶液的体积为V0mL,反应后三口烧瓶内溶液的体积为V1mL,实验条件下葡萄糖的转化率为___________ (用含V0和V1的代数式表示)。
④若滴定终点时俯视读数,对转化率的影响为___________ (填“偏高”“偏低”或“无影响”)。
Ⅲ.制备葡萄糖酸钙。
将CaCO3分散于适量蒸馏水中形成浊液,加入葡萄糖酸,至无CO2气体放出为止,煮沸,并趁热采用下图装置抽滤,滤掉未反应的CaCO3,得到澄清透明的葡萄糖酸钙溶液。
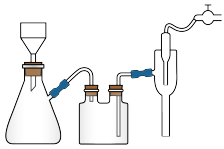
(4)抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是___________ 。
I.制备葡萄糖酸(装置如图所示)。

(1)仪器X的名称为

(2)滴入双氧水,水浴加热一段时间后,得到无色透明的葡萄糖酸溶液。反应的化学方程式为
Ⅱ.测定葡萄糖的转化率,确定合适的反应温度。
(3)用移液管取出三口烧瓶中的反应液2.00mL置于锥形瓶中,以酚酞作为指示剂并加20mL蒸馏水稀释,用0.04mol·L-1NaOH标准溶液滴定。
①滴定管使用的正确的操作顺序为蒸馏水洗涤→标准液润洗→
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②达到滴定终点时的现象为
③滴定过程消耗NaOH标准溶液的体积为V0mL,反应后三口烧瓶内溶液的体积为V1mL,实验条件下葡萄糖的转化率为
④若滴定终点时俯视读数,对转化率的影响为
Ⅲ.制备葡萄糖酸钙。
将CaCO3分散于适量蒸馏水中形成浊液,加入葡萄糖酸,至无CO2气体放出为止,煮沸,并趁热采用下图装置抽滤,滤掉未反应的CaCO3,得到澄清透明的葡萄糖酸钙溶液。

(4)抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是
2021·山东泰安·模拟预测
类题推荐
回答下列问题:
(1)用50mL0.55mol•L-1盐酸与50mL0.50mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
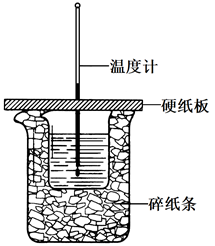
①从实验装置上看,尚缺少一种玻璃仪器,玻璃仪器的名称是__ 。
②若大烧杯上不盖硬纸板,求得的反应热△H__ (填“偏大”、“偏小”或“无影响”)。
③实验中若改用60mL0.50mol•L-1盐酸跟50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量(忽略测量误差,下同)__ (填“相等”或“不相等”),所求中和热__ (填“相等”或“不相等”)。
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热△H会__ (填“偏大”、“偏小”或“无影响”)。
Ⅱ.用0.1000mol•L-1的NaOH标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
(一)首先配制480mL0.1000mol•L-1的氢氧化钠溶液,有如下操作步骤:
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、__ 。需要用托盘天平称量NaOH固体的质量为__ g。
(3)若出现如下情况,所配溶液浓度将偏高的操作为__ 。
(二)用上述0.1000mol•L-1的NaOH标准溶液滴定未知浓度的盐酸溶液。
(4)步骤如下:
A.__ 。(补充所需操作)
B.分别用蒸馏水洗干净酸式滴定管和碱式滴定管。
C.用待测定的盐酸溶液润洗酸式滴定管。
D.用酸式滴定管取稀盐酸25.00mL,注入事先洗干净的锥形瓶中,加入指示剂。
E.碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至刻度“0”或“0”刻度以下。
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
G.另取锥形瓶,再重复操作一次。
(5)滴定实验所需的玻璃仪器有__ 。(填字母)
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸
(6)该小组同学选用酚酞做指示剂,滴定终点的现象为__ 。
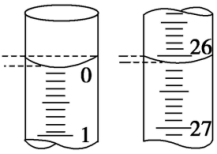
(7)该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为__ mL。
(8)该小组学生某3次实验的有关数据分别记录如表:
依据表中数据列式计算该HCl溶液的物质的量浓度为__ 。
(1)用50mL0.55mol•L-1盐酸与50mL0.50mol•L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

①从实验装置上看,尚缺少一种玻璃仪器,玻璃仪器的名称是
②若大烧杯上不盖硬纸板,求得的反应热△H
③实验中若改用60mL0.50mol•L-1盐酸跟50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量(忽略测量误差,下同)
④用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热△H会
Ⅱ.用0.1000mol•L-1的NaOH标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
(一)首先配制480mL0.1000mol•L-1的氢氧化钠溶液,有如下操作步骤:
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、
(3)若出现如下情况,所配溶液浓度将偏高的操作为
| A.容量瓶中原有少量蒸馏水 |
| B.转移溶液时,没有洗涤玻璃棒和溶解用的烧杯 |
| C.定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线 |
| D.定容时,俯视观察液面 |
(二)用上述0.1000mol•L-1的NaOH标准溶液滴定未知浓度的盐酸溶液。
(4)步骤如下:
A.
B.分别用蒸馏水洗干净酸式滴定管和碱式滴定管。
C.用待测定的盐酸溶液润洗酸式滴定管。
D.用酸式滴定管取稀盐酸25.00mL,注入事先洗干净的锥形瓶中,加入指示剂。
E.碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm,再把碱式滴定管固定好,排尽尖嘴部分的气泡,并调节液面至刻度“0”或“0”刻度以下。
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
G.另取锥形瓶,再重复操作一次。
(5)滴定实验所需的玻璃仪器有
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸
(6)该小组同学选用酚酞做指示剂,滴定终点的现象为
(7)该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为

(8)该小组学生某3次实验的有关数据分别记录如表:
| 滴定次数 | 待测HCl溶液的体积/mL | 0.1000mol•L-1NaOH的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 2.00 | 27.91 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网