单选题 较难0.4 引用3 组卷631
利用活性炭可以处理NO的污染,其原理为: 。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
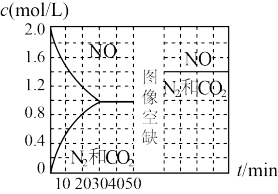

| A.0~10min的平均速率v(CO2)=0.1mol·L-1·min-1 |
| B.50min时改变的条件是升温 |
| C.若原平衡态压强为100kPa,维持体积不变,再通入一定量的CO2(g),达到平衡后压强变为150kPa,则平衡时NO转化了 |
| D.50min时改变的条件是加入高效的催化剂 |
2021·重庆·三模
类题推荐
利用活性炭还原法处理氮氧化物。有关反应为C(s)+2NO(g) N2(g)+ CO2(g) △H=akJ/mol。某研究小组向某恒容密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,已知在不同时间测得各物质的浓度如下:
N2(g)+ CO2(g) △H=akJ/mol。某研究小组向某恒容密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,已知在不同时间测得各物质的浓度如下:
(1)该反应的平衡常数表达式K=_______ ,在0~10s内,N2的平均反应速率为______ mol/(L·s),NO的转化率为________ ;
(2)30s后,改变某一条件,反应重新达到平衡,则改变的条件可能是________ ,若30s后升高温度至T2℃,平衡时,容器中NO的浓度由0.060mol/L变为0.072mol/L,则该反应的a___ 0 (填“>”、“<”或“=”)。
 N2(g)+ CO2(g) △H=akJ/mol。某研究小组向某恒容密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,已知在不同时间测得各物质的浓度如下:
N2(g)+ CO2(g) △H=akJ/mol。某研究小组向某恒容密闭容器中加入一定量的活性炭和NO,恒温(T1℃)条件下反应,已知在不同时间测得各物质的浓度如下:     | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 0.100 | 0.076 | 0.060 | 0.060 | 0.050 | 0.050 |
| N2 | 0 | 0.012 | 0.020 | 0.020 | 0.025 | 0.025 |
| CO2 | 0 | 0.012 | 0.020 | 0.020 | 0.011 | 0.011 |
(1)该反应的平衡常数表达式K=
(2)30s后,改变某一条件,反应重新达到平衡,则改变的条件可能是
高温下,向容积为2L的恒容密闭容器中加入一定量的CO2和足量的C,发生反应:C(s)+CO2(g) 2CO(g),CO2和CO的物质的量n随时间t的变化关系如图所示:
2CO(g),CO2和CO的物质的量n随时间t的变化关系如图所示:

(1)下列叙述能说明该反应已达到平衡状态的是_____ (填标号)。
(2)0~2min内,用CO表示的平均反应速率为_____ mol•L-1•min-1。
(3)2~3min内,该反应的平衡常数K=_____ 。
(4)3min末改变的条件是_____ ,再次达到平衡时测得容器内总压强为3MPa,此时,该反应的平衡常数Kp=_____ MPa(Kp为用平衡分压代替浓度的平衡常数,分压=总物质的量分数)。
(5)5min时再充入一定量的CO,则表示CO2的物质的量变化的曲线分别为_____ (填标号)。

(1)下列叙述能说明该反应已达到平衡状态的是
| A.容器内压强保持不变 |
| B.CO2(g)与CO(g)的物质的量之比为1:2 |
| C.气体的密度保持不变 |
| D.气体的平均相对分子质量保持不变 |
(3)2~3min内,该反应的平衡常数K=
(4)3min末改变的条件是
(5)5min时再充入一定量的CO,则表示CO2的物质的量变化的曲线分别为
用活性炭还原法处理氮氧化物,有关反应为:C(s)+ 2NO(g) N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
(1) 10 min~20 min的时间段内,以CO2表示的反应速率为____ ;
(2)计算出该反应的平衡常数的值K=________ ;
(3) 下列各项能作为判断该反应达到平衡状态的是____ (填序号字母);
A.容器内压强保持不变 B.2v正(NO)= v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是_____________ ;
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率__________ (填“增大”、 “不变”或“减小”)。
 N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g)。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:| 时间min/ 浓度mol·L-1 | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
(1) 10 min~20 min的时间段内,以CO2表示的反应速率为
(2)计算出该反应的平衡常数的值K=
(3) 下列各项能作为判断该反应达到平衡状态的是
A.容器内压强保持不变 B.2v正(NO)= v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
(4)30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是
(5)一定温度下,随着NO的起始浓度增大,则NO的平衡转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


