解答题-原理综合题 较易0.85 引用1 组卷443
CO2作为未米的重要碳源,其选择性加氢合成CH3OH一直是研究热点,在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g)∆H1<0
CH3OH(g)+H2O(g)∆H1<0
反应ii:CO2(g)+H2(g) CO(g)+H2O(g)△H2>0
CO(g)+H2O(g)△H2>0
(1)在特定温度下,由稳定态单质生成lmol化合物的焓变叫该物质在此温度下的标准生成焓(△fH )。表中为几种物质在298K的标准生成焓,则反应ii的∆H2=
)。表中为几种物质在298K的标准生成焓,则反应ii的∆H2=___ kJ·mol−1。
(2)若实验测得反应i:υ正=k正·c(CO2)·c3(H2),υ逆=k逆·c(CH3OH)·c(H2O)(k正、k逆为速率常数)。1899年阿仑尼乌斯指出化学反应速率常数和温度的定量关系为:k=A ,其中k为速率常数,A、R为常数,Ea为活化能,T为热力学温度,e为自然对数的底。则达到平衡后,仅加入催化剂,k正增大的倍数
,其中k为速率常数,A、R为常数,Ea为活化能,T为热力学温度,e为自然对数的底。则达到平衡后,仅加入催化剂,k正增大的倍数___ (填“>”“<”或“=")k逆增大的倍数。
(3)在CO2加氢合成CH3OH的体系中,下列说法错误的是___ (填标号).
A.增大H2浓度有利于提高CO2的转化率
B.若升高温度,反应i的正反应速率减小:反应ii的正反应速率增大
C.体系达平衡后,若压缩体积,则反应i平衡正向移动,反应ii平衡不移动
D.选用合适的催化剂可以提高CH3OH在单位时间内的产量
(4)某温度下,向容积为1L的密闭容器中通入2molCO2和10molH2,10min后体系达到平衡,此时CO2的转化率为20%,CH3OH的选择性为50%。
已知:CH3OH的选择性X= ×100%
×100%
①用CO2表示0~10min内平均反应速率υ(CO2)=___
②反应i的平衡常数K=___ L2/mol2(写出计算式即可)。
(5)维持压强和投料不变,将CO2和H2按一定流速通过反应器,二氧化碳的转化率a(CO2)和甲醇的选择性χ(CH3OH)随温度变化的关系如图所示:
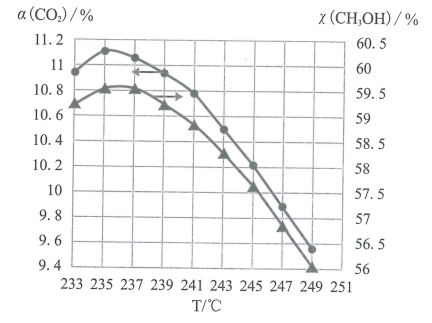
已知催化剂活性受温度影响变化不大,结合反应i和反应ii,分析235℃后曲线变化的原因。
①甲醇的选择性随温度升高而下降的原因是___ ;
②二氧化碳的转化率随温度升高也在下降的可能原因是___ 。
反应i:CO2(g)+3H2(g)
反应ii:CO2(g)+H2(g)
(1)在特定温度下,由稳定态单质生成lmol化合物的焓变叫该物质在此温度下的标准生成焓(△fH
| 物质 | H2(g) | CO2(g) | CO(g) | H2O(g) |
| △fH | 0 | −394 | −111 | −242 |
(2)若实验测得反应i:υ正=k正·c(CO2)·c3(H2),υ逆=k逆·c(CH3OH)·c(H2O)(k正、k逆为速率常数)。1899年阿仑尼乌斯指出化学反应速率常数和温度的定量关系为:k=A
(3)在CO2加氢合成CH3OH的体系中,下列说法错误的是
A.增大H2浓度有利于提高CO2的转化率
B.若升高温度,反应i的正反应速率减小:反应ii的正反应速率增大
C.体系达平衡后,若压缩体积,则反应i平衡正向移动,反应ii平衡不移动
D.选用合适的催化剂可以提高CH3OH在单位时间内的产量
(4)某温度下,向容积为1L的密闭容器中通入2molCO2和10molH2,10min后体系达到平衡,此时CO2的转化率为20%,CH3OH的选择性为50%。
已知:CH3OH的选择性X=
①用CO2表示0~10min内平均反应速率υ(CO2)=
②反应i的平衡常数K=
(5)维持压强和投料不变,将CO2和H2按一定流速通过反应器,二氧化碳的转化率a(CO2)和甲醇的选择性χ(CH3OH)随温度变化的关系如图所示:

已知催化剂活性受温度影响变化不大,结合反应i和反应ii,分析235℃后曲线变化的原因。
①甲醇的选择性随温度升高而下降的原因是
②二氧化碳的转化率随温度升高也在下降的可能原因是
2021·黑龙江哈尔滨·二模
类题推荐
减少CO2的排放、捕集并利用CO2是我国能源领域的一个重要战略方向。在CO2加氢合成甲醇的体系中,同时存在以下反应:
反应i:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-48.7 kJ·mol-1
反应ii:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
(1)在特定温度下,由稳定态单质生成1 mol化合物的焓变叫做该物质在此温度下的标准摩尔生成焓。表中为几种物质在298 K的标准生成焓,则反应ii的ΔH2(298K)=_______ kJ·mol-1。
(2)在CO2加氢合成甲醇的体系中,下列说法不正确的是_______ (填序号)。
(3)某温度下,向容积恒为1 L的密闭容器中通入1 mol CO2(g)和5 mol H2(g),10 min后体系达到平衡,此时CO2的转化率为20%,CH3OH的选择性为50%。
已知:CH3OH的选择性:χ= ×100%
×100%
①0-10 min内CO2的平均消耗速率v(CO2)=_______ 。
②反应i的平衡常数K=_______ (写出计算式即可)。
③反应ii的净速率v=v正-v逆=k正p(CO2)p(H2)-k逆p(CO)p(H2O),其中k正、k逆分别为正、逆反应的速率常数,p为气体的分压。降低温度时,k正-k逆_______ (选填“增大”、“减小”或“不变”)。
(4)维持压强、投料比和反应时间不变,将CO2和H2按一定流速通过反应器,CO2的转化率α(CO2)和甲醇的选择性x(CH3OH)随温度变化的关系如图所示。已知催化剂活性随温度影响变化不大,结合反应i和反应ii,分析下列问题:

①甲醇的选择性随温度升高而下降的原因_______ 。
②CO2的转化率随温度升高也下降的可能原因_______ 。
③不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是_______ (填序号)。
A.高温高压 B.高温低压 C.低温低压 D.低温高压
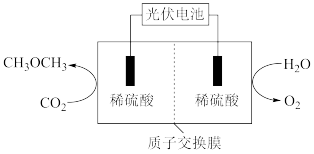
(5)科研人员通过电解酸化的CO2制备甲醚(CH3OCH3),装置如图所示。该电解过程中,阴极的电极反应式_______ 。
反应i:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-48.7 kJ·mol-1
反应ii:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
(1)在特定温度下,由稳定态单质生成1 mol化合物的焓变叫做该物质在此温度下的标准摩尔生成焓。表中为几种物质在298 K的标准生成焓,则反应ii的ΔH2(298K)=
| 物质 | H2(g) | CO2(g) | CO(g) | H2O(g) |
| 标准摩尔生成焓(kJ·mol-1) | 0 | -394 | -111 | -242 |
(2)在CO2加氢合成甲醇的体系中,下列说法不正确的是
| A.增大H2浓度有利于提高CO2的转化率 |
| B.若气体的平均相对分子质量不变,说明反应i、ii都已达平衡 |
| C.体系达平衡后,若压缩体积,反应i平衡正向移动,反应ii平衡不移动 |
| D.选用合适的催化剂可以提高甲醇在单位时间内的产量 |
已知:CH3OH的选择性:χ=
①0-10 min内CO2的平均消耗速率v(CO2)=
②反应i的平衡常数K=
③反应ii的净速率v=v正-v逆=k正p(CO2)p(H2)-k逆p(CO)p(H2O),其中k正、k逆分别为正、逆反应的速率常数,p为气体的分压。降低温度时,k正-k逆
(4)维持压强、投料比和反应时间不变,将CO2和H2按一定流速通过反应器,CO2的转化率α(CO2)和甲醇的选择性x(CH3OH)随温度变化的关系如图所示。已知催化剂活性随温度影响变化不大,结合反应i和反应ii,分析下列问题:

①甲醇的选择性随温度升高而下降的原因
②CO2的转化率随温度升高也下降的可能原因
③不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是
A.高温高压 B.高温低压 C.低温低压 D.低温高压
(5)科研人员通过电解酸化的CO2制备甲醚(CH3OCH3),装置如图所示。该电解过程中,阴极的电极反应式

减少CO2的排放、捕集并利用CO2是我国能源领域的一个重要战略方向。
在CO2加氢合成甲醇的体系中,同时存在以下反应:
反应ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-48.7kJ/mol
反应ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41kJ/mol
(1)反应ⅲ:CO(g)+2H2(g)=CH3OH(g)的△H3=_______ 。
(2)在CO2加氢合成甲醇的体系中,下列说法不正确的是_______(填序号)。
(3)某温度下,向容积恒为1L的密闭容器中通入lmolCO2(g)和5molH2(g),l0min后体系达到平衡,此时CO2的转化率为20%。CH3OH的选择性为50%。
已知:CH3OH的选择性: ×100%
×100%
①0~10min内CO2的平均消耗速率v(CO2)=_______ 。
②反应ⅰ的平衡常数K=_______ (写出计算式即可)。
③反应ⅱ的净速率v=v正-v逆=k正p(CO2)p(H2)-k逆p(CO)p(H2O),其中k正、k逆分别为正、逆反应的速率常数,p为气体的分压。降低温度时,k正-k逆_______ (选填“增大"、“减小”或“不变")。
(4)维持压强、投料比和反应时间不变,将CO2和H2按一定流速通过反应器,CO2的转化率 (CO2)和甲醇的选择性x(CH3OH)随温度变化的关系如图所示。已知催化剂活性随温度影响变化不大,结合反应ⅰ和反应ⅱ,分析下列问题:
(CO2)和甲醇的选择性x(CH3OH)随温度变化的关系如图所示。已知催化剂活性随温度影响变化不大,结合反应ⅰ和反应ⅱ,分析下列问题:

①甲醇的选择性随温度升高而下降的原因_______ ;CO2的转化率随温度升高也下降的可能原因是_______ 。
②不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是_______ (填序号)。
A.高温高压 B.高温低压 C低温低压 D.低温高压
在CO2加氢合成甲醇的体系中,同时存在以下反应:
反应ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-48.7kJ/mol
反应ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41kJ/mol
(1)反应ⅲ:CO(g)+2H2(g)=CH3OH(g)的△H3=
(2)在CO2加氢合成甲醇的体系中,下列说法不正确的是_______(填序号)。
| A.若在绝热恒容容器,反应ⅰ的平衡常数K保持不变,说明反应ⅰ、ⅱ都已达平衡 |
| B.若气体的平均相对分子质量不变,说明反应ⅰ、ⅱ都已达平衡 |
| C.体系达平衡后,若压缩体积,反应ⅰ平衡正向移动,反应ⅱ平衡不移动 |
| D.选用合适的催化剂可以提高甲醇在单位时间内的产量 |
(3)某温度下,向容积恒为1L的密闭容器中通入lmolCO2(g)和5molH2(g),l0min后体系达到平衡,此时CO2的转化率为20%。CH3OH的选择性为50%。
已知:CH3OH的选择性:
①0~10min内CO2的平均消耗速率v(CO2)=
②反应ⅰ的平衡常数K=
③反应ⅱ的净速率v=v正-v逆=k正p(CO2)p(H2)-k逆p(CO)p(H2O),其中k正、k逆分别为正、逆反应的速率常数,p为气体的分压。降低温度时,k正-k逆
(4)维持压强、投料比和反应时间不变,将CO2和H2按一定流速通过反应器,CO2的转化率

①甲醇的选择性随温度升高而下降的原因
②不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是
A.高温高压 B.高温低压 C低温低压 D.低温高压
CO2作为未来的重要碳源,其选择性加氢合成CH3OH一直是研究热点。在CO2加氢合成CH3OH的体系中,同时发生以下反应:
反应iCO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H1<0
CH3OH(g)+H2O(g) ∆H1<0
反应iiCO2(g)+H2(g) CO(g)+H2O(g) ∆H2>0
CO(g)+H2O(g) ∆H2>0
(1)已知化学键键能如表所示
上述反应i的ΔH1=_______ 。
(2)在T°C时,若某容器中只发生反应i,向体积为2L的恒容该容器中充入物质的量之和为4mol的H2和CO2,达到平衡时CO2的转化率与起始时 的关系如图所示:
的关系如图所示:

①当起始 时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)=
时,反应经过10min达到平衡,若此时CO2的转化率为0.6,则0~10min内平均反应速率v(H2)= _______ 。若此时再向容器中充入CO2(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将_______ (填“增大”“减小”或“不变”)。
②A、B、C、D四点中CH3OH的体积分数最大的点是_______ (填“A”、“B”“C”或“D”点)。
(3)如图所示,向甲乙两个密闭容器分别充入lmolCO2和3molH2,发生反应i,起始温度体积相同(T1℃、2L密闭容器)。达到平衡时,乙的容器容积为1.5L,则该温度下的平衡常数为_______ ,平衡时甲容器中CO2的物质的量_______ 0.5(填“大于、小于、等于、无法确定”),若将甲改为绝热恒容,其它条件不变,平衡时CH3OH的浓度将_______ (增大、减小、不变)。

(4)当起始 时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是
时,维持压强不变,将CO2和H2按一定流速通过反应器,催化剂活性受温度影响变化不大,结合反应i和反应ii,分析温度大于235℃后甲醇的选择性随温度升高而下降的原因是_______ 。

反应iCO2(g)+3H2(g)
反应iiCO2(g)+H2(g)
(1)已知化学键键能如表所示
| 化学键 | C=O | C-O | H-H | C-H | C-C | H-O |
| 键能/kJ·mol-1 | a | b | c | d | e | f |
上述反应i的ΔH1=
(2)在T°C时,若某容器中只发生反应i,向体积为2L的恒容该容器中充入物质的量之和为4mol的H2和CO2,达到平衡时CO2的转化率与起始时

①当起始
②A、B、C、D四点中CH3OH的体积分数最大的点是
(3)如图所示,向甲乙两个密闭容器分别充入lmolCO2和3molH2,发生反应i,起始温度体积相同(T1℃、2L密闭容器)。达到平衡时,乙的容器容积为1.5L,则该温度下的平衡常数为

(4)当起始

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


