解答题-工业流程题 适中0.65 引用1 组卷99
为了解决环境污染问题,中国政府大力扶持新能源汽车行业的发展。新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工艺流程如图:
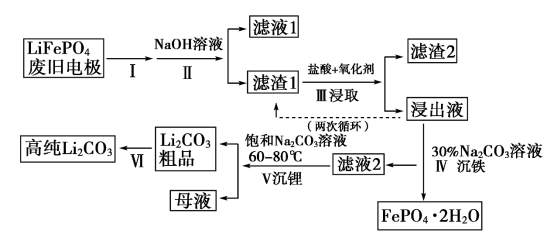
碳酸锂在水中溶解度:
(1)过程Ⅰ的操作是_______ 。
(2)过程Ⅱ加入足量NaOH溶液的作用是_______ (用化学方程式表示)。
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为_______ 。
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为_______ 。
(4)浸出液中存在大量H2PO 和HPO
和HPO ,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程Ⅳ:加入30%的Na2CO3溶液得到磷酸铁晶体的原因_______ 。

碳酸锂在水中溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/℃ | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程Ⅰ的操作是
(2)过程Ⅱ加入足量NaOH溶液的作用是
(3)过程Ⅲ采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如表所示:
| 序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | 滤渣中Li含量/% |
| 实验1 | HCl | H2O2 | 9.02 | 0.10 |
| 实验2 | HCl | NaClO3 | 9.05 | 0.08 |
| 实验3 | HCl | O2 | 7.05 | 0.93 |
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为
②综合考虑Li+的浸出率及环保因素,选择的氧化剂最好为
(4)浸出液中存在大量H2PO
2021高三·全国·专题练习
类题推荐
新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂( )做电极材料。对
)做电极材料。对 废旧电极(含杂质
废旧电极(含杂质 、石墨粉)回收并获得高纯
、石墨粉)回收并获得高纯 的工业流程图如下:
的工业流程图如下:
(1)过程ⅰ研磨粉碎的目的是___________ 。
(2)过程ⅱ加入足量 溶液的目的是除去
溶液的目的是除去 ,相关离子方程式为
,相关离子方程式为___________ 。
(3)过程ⅲ采用不同氧化剂分别进行实验,均采用 含量为3.7%的原料,控制
含量为3.7%的原料,控制 为3.5,浸取1.5h后,实验结果如下表所示:
为3.5,浸取1.5h后,实验结果如下表所示:
①实验2中, 能与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为
能与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为___________ 。
②过程ⅱ最终选择 作为氧化剂,原因是
作为氧化剂,原因是___________ 。
③过程ⅲ得到的浸出液循环两次的目的是___________ 。
(4)浸出液中存在大量 和
和 。结合
。结合平衡移动 原理,解释过程ⅳ得到磷酸铁晶体的原因___________ 。
(5)对比过程ⅳ和ⅴ,说明过程ⅳ不用饱和 溶液的原因:
溶液的原因:___________ 。
(6)过程ⅵ的操作为:将 粗品加水溶解,蒸发结晶至有大量固体析出,
粗品加水溶解,蒸发结晶至有大量固体析出,___________ 。

| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程ⅰ研磨粉碎的目的是
(2)过程ⅱ加入足量
(3)过程ⅲ采用不同氧化剂分别进行实验,均采用
| 序号 | 酸 | 氧化剂 | 浸出液中 | 滤渣中 |
| 实验1 | 9.02 | 0.10 | ||
| 实验2 | 9.05 | 0.08 | ||
| 实验3 | 7.05 | 0.93 |
②过程ⅱ最终选择
③过程ⅲ得到的浸出液循环两次的目的是
(4)浸出液中存在大量
(5)对比过程ⅳ和ⅴ,说明过程ⅳ不用饱和
(6)过程ⅵ的操作为:将
新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)作电极材料。对LiFePO4废旧电极(含杂质 A1、石墨粉)回收并获得高纯Li2CO3的工业流程图:
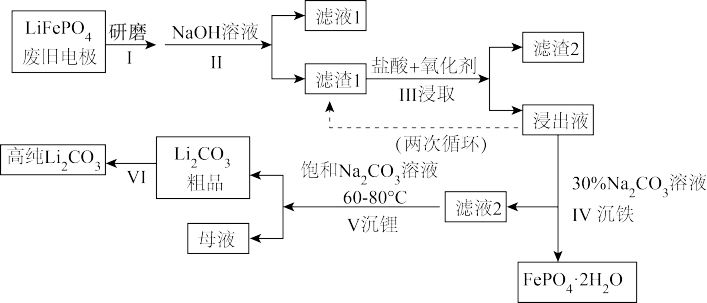
资料:碳酸锂在水中溶解度:
(1)“过程i”除研磨粉碎外,请再写出一种可以提高过程ii溶解速率的措施:____ 。
(2)“过程ii”加入足量 NaOH 溶液的离子反应方程式是________ 。
(3)“过程iii ”采用不同氧化剂分别进行实验,均采用 Li含量为3.7% 的原料,控制pH 为3.5,浸取1.5h后,实验结果如表所示:
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为_______ 。
②“过程iii”得到的浸出液循环两次的目的是________ 。
(4)浸出液中存在大量 H2PO4 -和 HPO ,已知:H2PO
,已知:H2PO ⇌HPO
⇌HPO +H+,HPO
+H+,HPO ⇌PO
⇌PO +H+,结合
+H+,结合平衡移动 原理,解释“过程iv”得到磷酸铁晶体的原因:___ 。
(5)“过程v”中,若“沉锂”中c(Li+ )=1.0mol·L-1,加入等体积饱和 Na2CO3溶液(浓度约为1.78mol/L),此时实验所得沉锂率为___ (已知Li2CO3的Ksp为9.0×10-4)。
(6)简述“过程vi”的操作:_________________ 。

资料:碳酸锂在水中溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(2)“过程ii”加入足量 NaOH 溶液的离子反应方程式是
(3)“过程iii ”采用不同氧化剂分别进行实验,均采用 Li含量为3.7% 的原料,控制pH 为3.5,浸取1.5h后,实验结果如表所示:
| 序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | ) 滤渣中Li含量/% |
| 实验1 | HCl | H2O2 | 9.02 | 0.10 |
| 实验2 | HCl | NaClO3 | 9.05 | 0.08 |
| 实验3 | HCl | O2 | 7.05 | 0.93 |
②“过程iii”得到的浸出液循环两次的目的是
(4)浸出液中存在大量 H2PO4 -和 HPO
(5)“过程v”中,若“沉锂”中c(Li+ )=1.0mol·L-1,加入等体积饱和 Na2CO3溶液(浓度约为1.78mol/L),此时实验所得沉锂率为
(6)简述“过程vi”的操作:
新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工业流程如图:
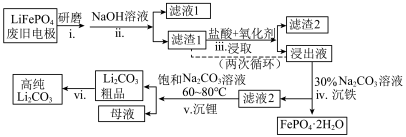
资料:碳酸锂在水中溶解度随温度变化如下:
(1)过程i研磨粉碎的目的是__________________ 。
(2)过程ii加入足量NaOH溶液的作用(用化学反应方程式表示)_________________ 。
(3)如过程iii采用NaClO3作为氧化剂,则过程中会反应会发生副反应生成黄绿色气体,
①该副反应对应的离子方程式为_______________________________________________________ ;
从环保角度分析,选择___________ (填字母)作为该过程的氧化剂会更好。
a.H2O2 b.浓硫酸 c.浓HNO3
②过程iii得到的浸出液循环两次的目的是________________________________________________ 。
(4)浸出液中存在大量H2PO4﹣和HPO42-,已知: ,结合平衡移动原理,解释过程iv得到磷酸铁晶体的原因
,结合平衡移动原理,解释过程iv得到磷酸铁晶体的原因______________________________________ 。
(5)简述过程vi的操作______________________________________________________________ 。

资料:碳酸锂在水中溶解度随温度变化如下:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程i研磨粉碎的目的是
(2)过程ii加入足量NaOH溶液的作用(用化学反应方程式表示)
(3)如过程iii采用NaClO3作为氧化剂,则过程中会反应会发生副反应生成黄绿色气体,
①该副反应对应的离子方程式为
从环保角度分析,选择
a.H2O2 b.浓硫酸 c.浓HNO3
②过程iii得到的浸出液循环两次的目的是
(4)浸出液中存在大量H2PO4﹣和HPO42-,已知:
(5)简述过程vi的操作
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


