解答题-原理综合题 适中0.65 引用1 组卷299
推进能源绿色转型,实现“碳达峰、碳中和”,事关经济社会发展全局。 甲烷化以及甲烷二氧化碳重整是能源综合利用领域的研究热点。
甲烷化以及甲烷二氧化碳重整是能源综合利用领域的研究热点。
(1)在一定温度和压力条件下,将按一定比例混合的 和
和 通过装有催化剂的反应器可得到
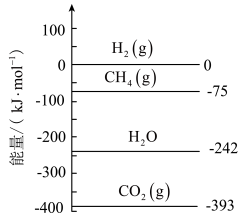
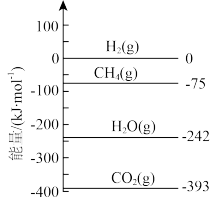
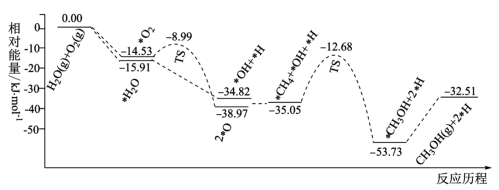
通过装有催化剂的反应器可得到 。298K时,相关物质的相对能量如下图,则该反应的热化学方程式为
。298K时,相关物质的相对能量如下图,则该反应的热化学方程式为___________ 。
(2)催化剂的选择是 甲烷化的核心,金属
甲烷化的核心,金属 或
或 均可作为催化剂。
均可作为催化剂。
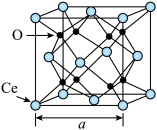
①催化剂 原子的基态核外电子的空间运动状态有
原子的基态核外电子的空间运动状态有___________ 种。
② 催化
催化 加
加 形成
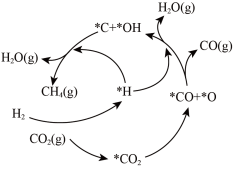
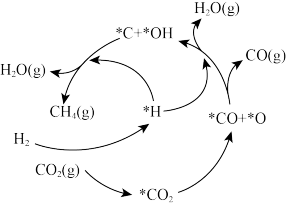
形成 的反应历程如图所示(吸附在催化剂表面的物种用*标注),存在的副反应的化学方程式为
的反应历程如图所示(吸附在催化剂表面的物种用*标注),存在的副反应的化学方程式为___________ ;
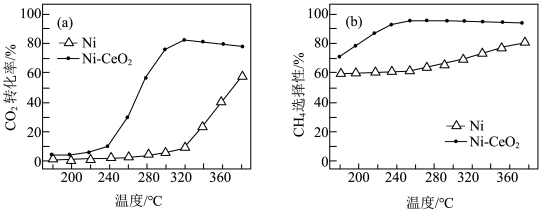
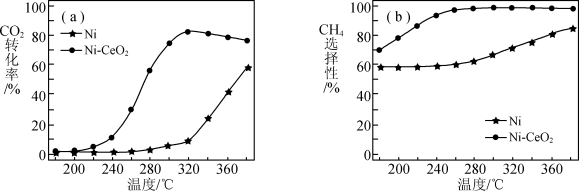
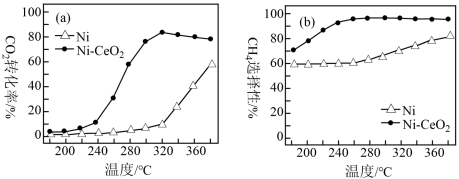
③上述两种不同催化剂的条件下反应相同时间,测得 转化率和生成
转化率和生成 选择性随温度变化影响如下图所示。高于320℃后,以
选择性随温度变化影响如下图所示。高于320℃后,以 为催化剂,
为催化剂, 转化率略有下降,而以
转化率略有下降,而以 为催化剂,
为催化剂, 转化率却仍在上升,其原因是;对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是
转化率却仍在上升,其原因是;对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是___________ 。
(3)甲烷与二氧化碳重整是一个复杂的反应体系,主要反应有:
反应Ⅰ:
反应Ⅱ:
反应III:
在一定条件下,1L恒容密闭容器中充入
 和
和
 ,测得
,测得 和
和 的平衡转化率分别为60%和20%,则该温度下反应Ⅰ的平衡常数
的平衡转化率分别为60%和20%,则该温度下反应Ⅰ的平衡常数
___________ ;若平衡时总压强为 ,则
,则
___________  。(分压
。(分压 总压
总压 物质的量分数)
物质的量分数)
(1)在一定温度和压力条件下,将按一定比例混合的

(2)催化剂的选择是
①催化剂
②

③上述两种不同催化剂的条件下反应相同时间,测得

(3)甲烷与二氧化碳重整是一个复杂的反应体系,主要反应有:
反应Ⅰ:
反应Ⅱ:
反应III:
在一定条件下,1L恒容密闭容器中充入
2021·辽宁沈阳·三模
类题推荐
推进能源绿色转型,实现碳达峰、碳中和,事关经济社会发展全局。CO2甲烷化及甲烷重整制甲醇是能源综合利用领域的研究热点。回答下列问题:
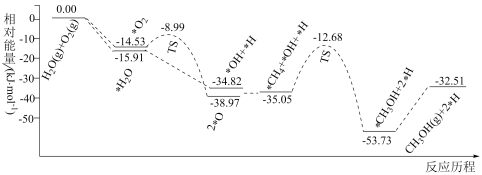
(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+ O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是_____ (填标号)。
(2)催化剂的选择是CO2甲烷化的核心,金属Ni或Ni-CeO2均可作为催化剂。
①基态Ni原子的核外电子排布式为_____ 。
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是____ 。对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是____ 。
(3)一定条件下,发生反应CO(g)+3H2(g) CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=
CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m= ]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。
]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。

①图中m1、m2、m3由大到小的顺序为_____ 。
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=____ mol•L-1•s-1。平衡时k正:k逆=____ ,达到平衡后,升高温度,k正:k逆_____ (填“增大”、“减小”或“不变”)。
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为____ 。

(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+

| A.该反应的△H=-32.5kJ•mol-1 |
| B.H2O(g)比O2(g)更容易吸附在催化剂表面 |
| C.该反应过程中只涉及σ键的断裂与形成 |
| D.图中慢反应的化学方程式为*CH4+*OH=*CH3OH+*H |
①基态Ni原子的核外电子排布式为
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是

(3)一定条件下,发生反应CO(g)+3H2(g)

①图中m1、m2、m3由大到小的顺序为
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为

习近平总书记在二十大报告中提出“中国式现代化是人与自然和谐共生的现代化”。 甲烷化及甲烷重整制甲醇是绿色能源的研究热点。回答下列问题。
甲烷化及甲烷重整制甲醇是绿色能源的研究热点。回答下列问题。
(1)已知 、
、 和
和 (
( 的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:
的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:
 ,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,
,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注, 代表过渡态)。下列说法正确的是___________(填标号)。
代表过渡态)。下列说法正确的是___________(填标号)。
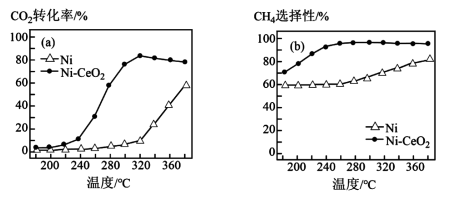
(2)催化剂的选择是 甲烷化的核心,金属
甲烷化的核心,金属 或
或 均可作为催化剂。在其他条件相同时,两种催化剂与
均可作为催化剂。在其他条件相同时,两种催化剂与 转化率和
转化率和 选择性随温度的变化关系如图所示。高于320℃,以
选择性随温度的变化关系如图所示。高于320℃,以 为催化剂,
为催化剂, 转化率略有下降,而以
转化率略有下降,而以 为催化剂,
为催化剂, 转化率却仍在上升,其原因是
转化率却仍在上升,其原因是___________ 。对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是___________ 。
(3)一定条件下,发生反应 ,测
,测 的平衡转化率与温度、起始投料比
的平衡转化率与温度、起始投料比 的关系如图所示。已知
的关系如图所示。已知 ,
, (
( 、
、 为速率常数)。
为速率常数)。
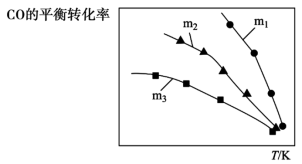
①图中 、
、 、
、 由大到小的顺序为
由大到小的顺序为___________ 。
②在一定温度下,向 的密闭容器中充入
的密闭容器中充入 和
和 ,经
,经 达到平衡,此时
达到平衡,此时 的转化率为50%。
的转化率为50%。 内,
内,
___________  。平衡时
。平衡时
___________ 。
(1)已知

| A.该反应的 |
| B. |
| C.该反应过程中只涉及极性键的断裂与形成 |
| D.图中慢反应的化学方程式为 |

(3)一定条件下,发生反应

①图中
②在一定温度下,向
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网