解答题-实验探究题 适中0.65 引用1 组卷272
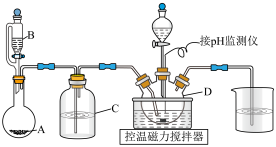
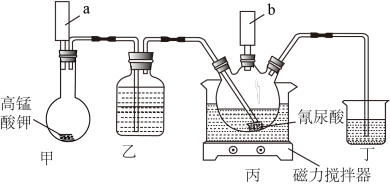
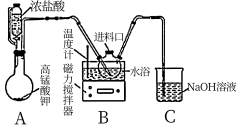
二氯异氰尿酸钠(简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冰水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
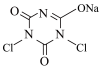
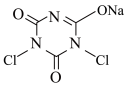
 +2NaClO(浓)
+2NaClO(浓) 
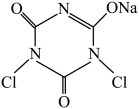
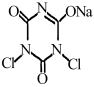 +2NaOH+H2O
+2NaOH+H2O
实验步骤如下:
Ⅰ.制备高浓度NaClO溶液
从进料口加入10mL 30% NaOH溶液,在10℃左右水浴,搅拌条件下通入Cl2至溶液pH约为8;再加入10mL 40% NaOH溶液,继续通入Cl2至溶液pH约为8。
(1)用烧碱固体配制40%的NaOH溶液,下列仪器中不需要的是___________ (写名称)。
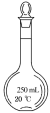
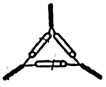

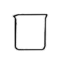
(2)“步骤I”测定溶液pH的方法是___________ 。
(3)水浴降温可以减少NaClO3副产物的生成,该副反应的离子方程式为___________ 。
(4)通过改进实验装置,可以提高B中NaOH的利用率,可行的方法是___________ (写一种)。
Ⅱ.制备二氯异氰尿酸钠
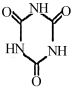
待步骤Ⅰ结束后,从进料口加入氰尿酸,在搅拌状态下继续通入Cl2,在10℃左右下反应30min,此时三颈瓶内有DCCNa白色晶体析出,停止反应。
(5)为了使晶体充分析出并分离,需要的操作为___________ 、___________ 洗涤、干燥。
(6)继续通入Cl2的目的是___________ 。
Ⅲ.二氯异氰尿酸钠有效氯含量测定
称取0.1000g样品,用100mL蒸馏水于碘量瓶中溶解后,依次加入20mL 0.3mol·L-1醋酸溶液和过量的KI溶液。用0.1000 mol·L-1 Na2S2O3溶液滴定至溶液呈浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液16.00mL。
(已知: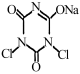

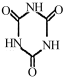
 ,
, )
)
(7)滴定终点的现象为___________ 。
(8)样品有效氯=___________ 。( )
)

 +2NaClO(浓)
+2NaClO(浓)  +2NaOH+H2O
+2NaOH+H2O实验步骤如下:
Ⅰ.制备高浓度NaClO溶液
从进料口加入10mL 30% NaOH溶液,在10℃左右水浴,搅拌条件下通入Cl2至溶液pH约为8;再加入10mL 40% NaOH溶液,继续通入Cl2至溶液pH约为8。
(1)用烧碱固体配制40%的NaOH溶液,下列仪器中不需要的是




(2)“步骤I”测定溶液pH的方法是
(3)水浴降温可以减少NaClO3副产物的生成,该副反应的离子方程式为
(4)通过改进实验装置,可以提高B中NaOH的利用率,可行的方法是
Ⅱ.制备二氯异氰尿酸钠
待步骤Ⅰ结束后,从进料口加入氰尿酸,在搅拌状态下继续通入Cl2,在10℃左右下反应30min,此时三颈瓶内有DCCNa白色晶体析出,停止反应。
(5)为了使晶体充分析出并分离,需要的操作为
(6)继续通入Cl2的目的是
Ⅲ.二氯异氰尿酸钠有效氯含量测定
称取0.1000g样品,用100mL蒸馏水于碘量瓶中溶解后,依次加入20mL 0.3mol·L-1醋酸溶液和过量的KI溶液。用0.1000 mol·L-1 Na2S2O3溶液滴定至溶液呈浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液16.00mL。
(已知:


(7)滴定终点的现象为
(8)样品有效氯=
2021·福建龙岩·三模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
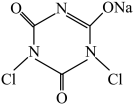 ,简称
,简称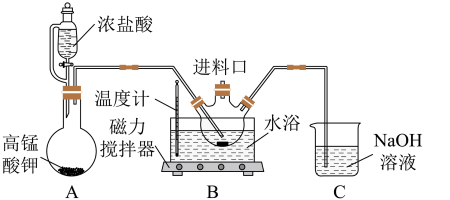
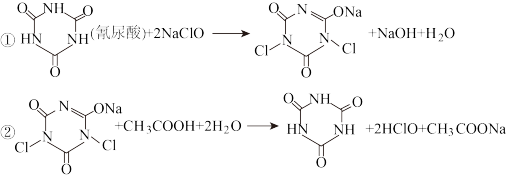
 (氰尿酸)+2NaClO
(氰尿酸)+2NaClO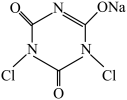 +NaOH+H2O
+NaOH+H2O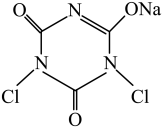 +CH3COOH+2H2O
+CH3COOH+2H2O +2HClO+ CH3COONa
+2HClO+ CH3COONa