解答题-实验探究题 适中0.65 引用1 组卷158
Ⅰ.某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计了如图所示的实验装置:
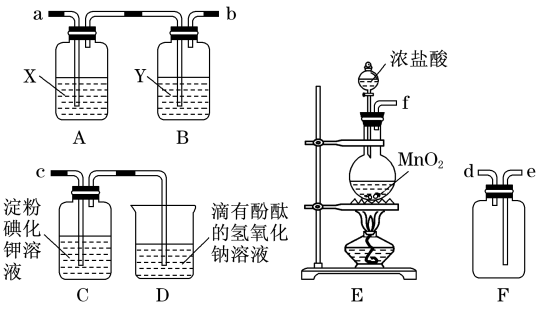
请回答下列问题:
(1)整套实验装置的连接顺序是f接接接(各接口处的字母代号)。___________
(2)E装置中制取氯气的离子方程式是___________ 。
(3)B装置的作用是___________ ;A装置中试剂X是___________ 。
(4)C装置中可观察到的现象是___________ 。
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
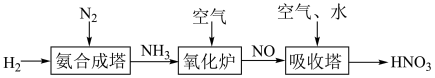
(1)下列有关NH3的说法,不正确 的是___________ (填字母)。
A.工业合成NH3需要铁触媒 B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥 D.NH3受热易分解,须置于冷暗处保存
(2)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________ mol∙L-1。
(3)氨气在氧化炉中所发生反应的化学方程式为___________ 。
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为:Na2CO3+2NO2=NaNO3+___________+CO2(请完成化学方程式)。___________
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ 。

请回答下列问题:
(1)整套实验装置的连接顺序是f接接接(各接口处的字母代号)。
(2)E装置中制取氯气的离子方程式是
(3)B装置的作用是
(4)C装置中可观察到的现象是
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
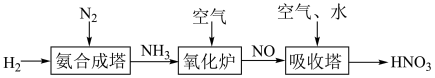
(1)下列有关NH3的说法,
A.工业合成NH3需要铁触媒 B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥 D.NH3受热易分解,须置于冷暗处保存
(2)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
(3)氨气在氧化炉中所发生反应的化学方程式为
(4)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为:Na2CO3+2NO2=NaNO3+___________+CO2(请完成化学方程式)。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
20-21高二下·四川眉山·阶段练习
类题推荐
氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
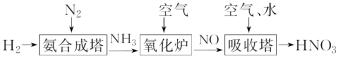
(1)下列有关NH3的说法中,不正确的是___________(双选,填标号)。
(2)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________ mol·L-1。
(3)氨气燃烧的化学方程式为___________ 。
(4)HNO3是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的___________ 性。
(5)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为Na2CO3+2NO2=NaNO3+___________ +CO2(请填写完成化学方程式)。
②氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol 的混合气体完全转化为N2则混合气体中NO和NO2的物质的量之比为___________ ,若用通式NOx表示氮氧化物,则每摩尔氨可将___________ mol的NOx转化为N2。

(1)下列有关NH3的说法中,不正确的是___________(双选,填标号)。
| A.工业合成NH3需要在高温高压催化剂下进行 |
| B.NH3可用来生产碳铵和尿素等化肥 |
| C.NH3可用浓硫酸或无水氯化钙干燥 |
| D.NH3受热易分解,须置于冷暗处保存 |
(3)氨气燃烧的化学方程式为
(4)HNO3是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的
(5)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为Na2CO3+2NO2=NaNO3+
②氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol 的混合气体完全转化为N2则混合气体中NO和NO2的物质的量之比为
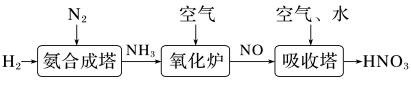
氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
(2)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________ mol·L-1。
(3)氨气催化氧化形成NO的化学方程式为___________ 。
(4)HNO3是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的___________ 性。
(5)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为Na2CO3+2NO2=NaNO3+___________ +CO2(完成化学方程式)。
②氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为___________ ,若用通式NOx表示氮氧化物,则每摩尔氨可将___________ mol的NOx转化为N2。
| A.工业合成NH3需要在高温、高压、催化剂下进行 |
| B.NH3可用来生产碳铵和尿素等化肥 |
| C.NH3可用浓硫酸或无水氯化钙干燥 |
| D.NH3受热易分解,须置于冷暗处保存 |
(3)氨气催化氧化形成NO的化学方程式为
(4)HNO3是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的
(5)“吸收塔” 尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO2的反应原理为Na2CO3+2NO2=NaNO3+
②氨转化法。已知7 mol氨恰好能将含NO和NO2共6 mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
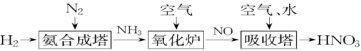
氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题: 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。
(2) 易溶于水,标准状况下,用充满
易溶于水,标准状况下,用充满 的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________  。
。
(3)氨气燃烧的化学方程式为___________ 。
(4) 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的
是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的___________ 性。
(5)“吸收塔”尾部会有含NO、 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。
纯碱溶液与 反应的原理为
反应的原理为
___________  (请填写完成化学方程式,已配平)。
(请填写完成化学方程式,已配平)。
②氨转化法。
已知7mol氨恰好能将含NO和 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为___________ ,若用通式 表示氮氧化物,则每摩尔氨可将
表示氮氧化物,则每摩尔氨可将___________ mol的 转化为
转化为 。
。
(6)工业上可采用碱液吸收和氨还原处理含 尾气,其中用碱液吸收的化学方程式为
尾气,其中用碱液吸收的化学方程式为 ,
, 。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。
。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。
| A.工业合成 |
| B. |
| C. |
| D. |
(3)氨气燃烧的化学方程式为
(4)
(5)“吸收塔”尾部会有含NO、
①纯碱溶液吸收法。
纯碱溶液与
②氨转化法。
已知7mol氨恰好能将含NO和
(6)工业上可采用碱液吸收和氨还原处理含
| A.1mol | B.1mol NO和4mol |
| C.1mol | D.4mol NO和4mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


