解答题-工业流程题 适中0.65 引用7 组卷696
氯化亚铜(CuCl)可用作有机合成的催化剂,CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液(CuCl+Cl- CuCl
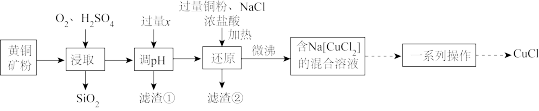
CuCl ),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
),在潮湿空气中易水解、易氧化。工业上用黄铜矿(主要成分是CuFeS2,还含有少量的SiO2)制备CuCl的工艺流程如图:
25℃时,相关物质的Ksp见表。
回答下列问题:
(1)黄铜矿预先粉碎的目的是_______ 。
(2)调pH加入的过量x为_______ (填化学式),滤渣①的成分_______ (填化学式)。
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为_______ 。
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为_______ 。
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
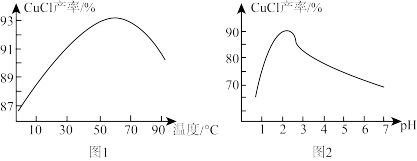
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式_______ 。
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为_______ (结果保留三位有效数字)。

25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | CuCl |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-19.7 | 1×10-5.9 |
(1)黄铜矿预先粉碎的目的是
(2)调pH加入的过量x为
(3)“还原”时,铜粉转化为Na[CuCl2]的离子反应方程式为
(4)已知:温度、pH对CuCl产率的影响如图1、图2所示。则析出CuCl晶体的最佳条件为
A.温度在60℃左右pH为2.0~2.5 B.温度在90℃左右pH为2.0~2.5
C.温度在60℃左右pH为5.0~6.0 D.温度在90℃左右pH为5.0~6.0
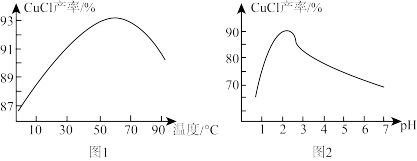
(5)析出的氯化亚铜晶体要立即用无水乙醇洗涤,“醇洗”可快速除去滤渣表面的水,防止滤渣被空气氧化为碱式氯化铜[Cu2(OH)3Cl]。写出氯化亚铜被氧化为碱式氯化铜的化学反应方程式
(6)粗产品中氯化亚铜含量的测定:
①称取样品3.0 g于锥形瓶中,再加入过量的FeCl3溶液充分溶解,配制250 mL溶液。②从中取出25.00mL溶液,用0.1000 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+。
三次平行实验,到达滴定终点时,消耗硫酸铈标准溶液的体积分别为26.05 mL、24.05 mL、23.95 mL。则样品中CuCl的纯度为
2021·黑龙江大庆·二模
类题推荐
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在潮湿空气中易水解氧化;见光则分解,变成褐色;CuCl难溶于醇和水,可溶于氯离子浓度较大的体系。下图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)

根据以上信息回答下列问题:
(1)写出生产过程中所用物质的名称:____________ ,________________ 。
(2)写出产生CuCl的化学方程式:________________________________ 。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由________________________________________________ 。实际生产中SO2要适当过量,原因可能是___ (答一点即可).
(4)得到CuC1晶体后,还需要经过水洗、乙醇洗涤两步操作。用乙醇洗涤的作用是________________ 。
(5)实验探究pH对CuCl产率的影响如下表所示:
析出CuCl晶体最佳pH为_________ ,当pH较大时CuCl产率变低原因是________________ 。
(6)氯化亚铜的定量分析:
①称取样品0.25g和过量的FeCl3溶液于250mL锥形瓶中,充分溶解。
②用0.10mol•L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3═CuCl2+FeCl2、Fe2++Ce4+═Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为_______________ (结果保留三位有效数字)。

根据以上信息回答下列问题:
(1)写出生产过程中所用物质的名称:
(2)写出产生CuCl的化学方程式:
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由
(4)得到CuC1晶体后,还需要经过水洗、乙醇洗涤两步操作。用乙醇洗涤的作用是
(5)实验探究pH对CuCl产率的影响如下表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率 | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
(6)氯化亚铜的定量分析:
①称取样品0.25g和过量的FeCl3溶液于250mL锥形瓶中,充分溶解。
②用0.10mol•L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3═CuCl2+FeCl2、Fe2++Ce4+═Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
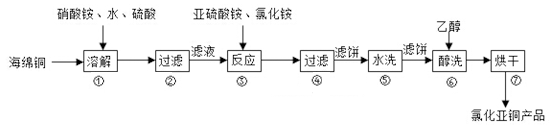
氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下图所示。
回答下列问题:
(1)CuCl中Cu元素在周期表中的位置为___________ 。
(2)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为________ 。溶解温度应控制在60~70℃,原因是______________ 。
(3)写出步骤③中主要反应的离子方程式________ 。(NH4)2SO3要适当过量,目的有:保证Cu2+的还原速率,__________ 。已知NH4Cl、Cu2+的物质的量之比 与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是
与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是________ 。
(4)步骤⑥加入乙醇洗涤的目的是__________ 。
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解;
②用0.100mol·L-1硫酸铈[Ce(SO4)2]标准溶液测定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
则样品中CuCl的纯度为_______ (结果保留3位有效数字)。
回答下列问题:
(1)CuCl中Cu元素在周期表中的位置为
(2)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为
(3)写出步骤③中主要反应的离子方程式
 与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是
与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定浓度后氯化亚铜的沉淀率减少,原因是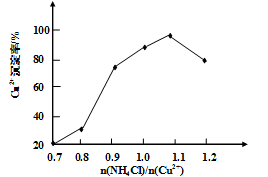
(4)步骤⑥加入乙醇洗涤的目的是
(5)氯化亚铜的定量分析:
①称取样品0.250g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解;
②用0.100mol·L-1硫酸铈[Ce(SO4)2]标准溶液测定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。
三次平衡实验结果如下表(平衡实验结果相差不能超过1%):
| 平衡实验次数 | 1 | 2 | 3 |
| 0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化变成绿色;见光分解变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl−)生产CuCl的流程:
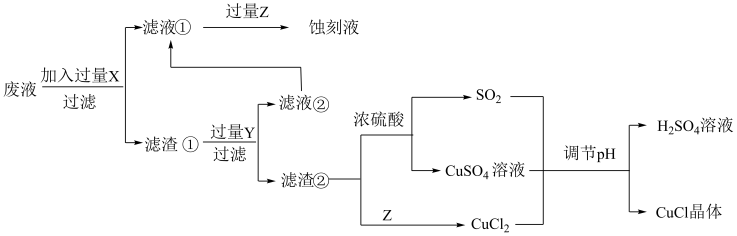
根据以上信息回答下列问题:
(1)生产过程中X的化学式为____ 。
(2)写出产生CuCl的离子方程式:____ 。
(3)实验探究pH对CuCl产率的影响如表所示:
析出CuCl晶体最佳pH为____ ,当pH较大时CuCl产率变低原因是____ 。调节pH时,___ (填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是____ 。
(4)氯化亚铜的定量分析:
①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10mol·L−1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如表(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为_____ 。(结果保留三位有效数字)。
(5)由CuCl水解再热分解可得到纳米Cu2O。第一步CuCl水解的离子方程式为:CuCl(s)+H2O(l) CuOH(s)+Cl− (aq)+H+(aq),第二步CuOH热分解的化学方程式为
CuOH(s)+Cl− (aq)+H+(aq),第二步CuOH热分解的化学方程式为____ 。第一步CuCl水解反应的平衡常数K与此温度下KW、Ksp(CuOH)、Ksp(CuCl)的关系为K=____ 。

根据以上信息回答下列问题:
(1)生产过程中X的化学式为
(2)写出产生CuCl的离子方程式:
(3)实验探究pH对CuCl产率的影响如表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
(4)氯化亚铜的定量分析:
①称取样品0.25g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10mol·L−1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如表(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
(5)由CuCl水解再热分解可得到纳米Cu2O。第一步CuCl水解的离子方程式为:CuCl(s)+H2O(l)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


