解答题-原理综合题 适中0.65 引用1 组卷135
将CO2应用于生产清洁燃料甲醇,既能缓解温室效应的影响,又能为能源的制备开辟新的渠道,其合成反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。回答下列问题:
(1)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)⇌CH3NH2(g)+H2O(g) ∆H,已知该反应中相关化学键的键能数据如下:
则该反应的∆H=_______ kJ•mol-1。
(2)汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。已知:
①CO(g)+NO2(g)⇌CO2(g)+NO(g) ∆H1=-226kJ•rnol-1
②N2(g)+2O2(g)⇌2NO2(g) ∆H2=+68kJ•mol-1
③N2(g)+O2(g)⇌2NO(g) ∆H3=+183kJ•mol-1
则:CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_______ 。
(3)CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
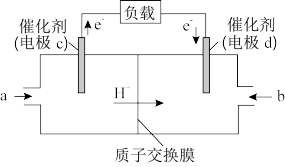
电池总反应为2CH3OH+3O2=2CO2+4H2O。则d电极是_______ (填“正极”或“负极”),c电极的电极反应式为______ 。若线路中转移2mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为_____ L。
(1)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)⇌CH3NH2(g)+H2O(g) ∆H,已知该反应中相关化学键的键能数据如下:
| 共价键 | C-O | H-O | N-H | C-N |
| 键能/kJ•mol-1 | 351 | 463 | 393 | 293 |
则该反应的∆H=
(2)汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。已知:
①CO(g)+NO2(g)⇌CO2(g)+NO(g) ∆H1=-226kJ•rnol-1
②N2(g)+2O2(g)⇌2NO2(g) ∆H2=+68kJ•mol-1
③N2(g)+O2(g)⇌2NO(g) ∆H3=+183kJ•mol-1
则:CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是
(3)CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2=2CO2+4H2O。则d电极是
20-21高一下·山东潍坊·阶段练习
类题推荐
Ⅰ.常温下,pH=1的某溶液A中含有NH 、K+、Na+、Fe3+、Al3+、Fe2+、CO
、K+、Na+、Fe3+、Al3+、Fe2+、CO 、NO
、NO 、Cl—、I—、SO
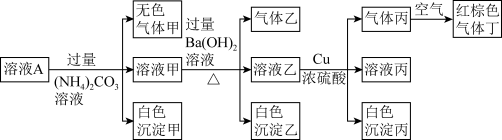
、Cl—、I—、SO 中的四种离子,且各离子的物质的量浓度均为0.1 mol·L-1。现取该溶液进行有关实验,实验结果如图所示:
中的四种离子,且各离子的物质的量浓度均为0.1 mol·L-1。现取该溶液进行有关实验,实验结果如图所示:___________ 。
A.溶液A为无色溶液
B.实验消耗Cu 14.4 g,则生成气体丙的体积为3.36 L
C.生成的甲、乙、丙气体均为无色难溶于水的气体
D.溶液A中一定没有CO 和I-
和I-
E.白色沉淀乙只有BaCO3,白色沉淀丙只有BaSO4
(2)写出生成白色沉淀甲的离子方程式:___________ 。
(3)溶液A中除氢离子外,一定含有的四种离子是___________ 。
(4)溶液甲中阳离子(H+除外)的检验方法是___________ 。
Ⅱ.将CO2应用于生产清洁燃料甲醇,既能缓解温室效应的影响,又能为能源的制备开辟新的渠道,其合成反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。回答下列问题:
CH3OH(g)+H2O(g)。回答下列问题:
(5)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g)△H。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g)△H。已知该反应中相关化学键的键能数据如下:
则该反应的△H=___________ kJ•mol-1。
(6)已知:CO(g)+NO2(g) CO2(g)+NO(g)△H1=-226kJ•rnol-1
CO2(g)+NO(g)△H1=-226kJ•rnol-1
N2(g)+2O2(g) 2NO2(g)△H2=+68kJ•mol-1
2NO2(g)△H2=+68kJ•mol-1
N2(g)+O2(g) 2NO(g)△H3=+183kJ•mol-1
2NO(g)△H3=+183kJ•mol-1
则CO与NO反应生成CO2气体和N2气体的热化学方程式为___________
A.溶液A为无色溶液
B.实验消耗Cu 14.4 g,则生成气体丙的体积为3.36 L
C.生成的甲、乙、丙气体均为无色难溶于水的气体
D.溶液A中一定没有CO
E.白色沉淀乙只有BaCO3,白色沉淀丙只有BaSO4
(2)写出生成白色沉淀甲的离子方程式:
(3)溶液A中除氢离子外,一定含有的四种离子是
(4)溶液甲中阳离子(H+除外)的检验方法是
Ⅱ.将CO2应用于生产清洁燃料甲醇,既能缓解温室效应的影响,又能为能源的制备开辟新的渠道,其合成反应为CO2(g)+3H2(g)
(5)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)
| 共价键 | C—O | H—O | N—H | C—N |
| 键能/kJ•mol-1 | 351 | 463 | 393 | 293 |
(6)已知:CO(g)+NO2(g)
N2(g)+2O2(g)
N2(g)+O2(g)
则CO与NO反应生成CO2气体和N2气体的热化学方程式为
甲醇既是重要的化工原料,又可作为燃料,还可以作为燃料电池的原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下: CO(g)+2H2(g)⇌CH3OH(g) ΔH (已知:CO的结构与N2相似)回答下列问题:
(1)已知反应中相关的化学键键能数据如下:
由此计算ΔH=_______ kJ·mol-1
(2)工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)⇌CH3OH(g) △H1=﹣90.7kJ·mol-1①
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H2=﹣23.5kJ·mol-1②
CO(g)+H2O(g)⇌CO2(g)+H2(g) △H3=﹣41.2kJ·mol-1③
反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的△H=_______ 。
(3)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO 还原为N2,一段时间后,溶液的碱性明显增强.则该反应离子方程式为
还原为N2,一段时间后,溶液的碱性明显增强.则该反应离子方程式为_______ 。
②电化学降解NO 的原理如图所示,电源正极为
的原理如图所示,电源正极为_______ (填“A”或“B”),若总反应4NO +4H+═5O2+2N2+2H2O,则阴极反应式为
+4H+═5O2+2N2+2H2O,则阴极反应式为_______ 。

③能否把质子交换膜改为阴离子交换膜_______ 。(填“能”或“不能”)
(1)已知反应中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(KJ/mol) | 436 | 343 | 1076 | 465 | 413 |
(2)工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用下进行的,反应器中发生了下列反应:
CO(g)+2H2(g)⇌CH3OH(g) △H1=﹣90.7kJ·mol-1①
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H2=﹣23.5kJ·mol-1②
CO(g)+H2O(g)⇌CO2(g)+H2(g) △H3=﹣41.2kJ·mol-1③
反应器中的总反应可表示为3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),计算该反应的△H=
(3)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO
②电化学降解NO

③能否把质子交换膜改为阴离子交换膜
将CO2应用于生产清洁燃料甲醇,既能缓解温室效应的影响,又能为能源的制备开辟新的渠道,其合成反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。回答下列问题:
CH3OH(g)+H2O(g)。回答下列问题:
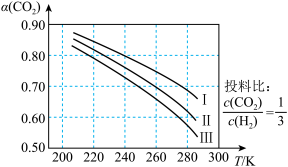
(1)如图为CO2平衡转化率和温度、压强的关系,其中压强分别为3.0MPa、4.0MPa和5.0MPa。据图可知,该反应为_______________ 反应(填“放热”或“吸热")。设CO2的初始浓度为comol•L-1,根据5.0MPa时的数据计算该反应的平衡常数K(240k)=_______________ (列出计算式即可)。若在4.0MPa时减小投料比,则CO2的平衡转化率曲线可能位于II线的_______________ (填“上方”或“下方”)。
(2)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g)△H。已知该反应中相关化学键的键能数据如下
CH3NH2(g)+H2O(g)△H。已知该反应中相关化学键的键能数据如下
则该反应的△H=_______________ k.J•mol-1 。
(3)已知:①CO(g)+NO2(g) CO2(g)+NO(g) △H1=-226kJ•rnol-1
CO2(g)+NO(g) △H1=-226kJ•rnol-1
②N2(g)+2O2(g) 2NO2(g)△H2=+68kJ•mol-1
2NO2(g)△H2=+68kJ•mol-1
③N2(g)+O2(g) 2NO(g) △H3=+183kJ•mol-1
2NO(g) △H3=+183kJ•mol-1
则:2CO(g)+2NO(g) 2CO2(g)+N2(g) △H=
2CO2(g)+N2(g) △H=_______________ kJ•mol-1。
(4)一定温度下,下列措施一定能加快反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)的速率的是
CH3OH(g)+H2O(g)的速率的是_______________ (填选项字母)。
A.及时移去甲醇 B.改进催化剂 C.提高反应物浓度 D.增大容器压强
(5)甲烷重整可选氧化物NiO- Al2O3作为催化剂,工业上常用Ni(NO3)2、Al(NO3)3混合液加入氨水调节pH=12(常温),然后将浊液高压恒温放置及煅烧等操作制备该催化剂。加入氨水调节pH=12时,c(Ni2+)为_______________ 。[已知:Ksp[Ni(OH)2]=5×10-16]
(1)如图为CO2平衡转化率和温度、压强的关系,其中压强分别为3.0MPa、4.0MPa和5.0MPa。据图可知,该反应为

(2)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)
| 共价键 | C—O | H—O | N—H | C—N |
| 键能/k.J•mol-1 | 351 | 463 | 393 | 293 |
(3)已知:①CO(g)+NO2(g)
②N2(g)+2O2(g)
③N2(g)+O2(g)
则:2CO(g)+2NO(g)
(4)一定温度下,下列措施一定能加快反应CO2(g)+3H2(g)
A.及时移去甲醇 B.改进催化剂 C.提高反应物浓度 D.增大容器压强
(5)甲烷重整可选氧化物NiO- Al2O3作为催化剂,工业上常用Ni(NO3)2、Al(NO3)3混合液加入氨水调节pH=12(常温),然后将浊液高压恒温放置及煅烧等操作制备该催化剂。加入氨水调节pH=12时,c(Ni2+)为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


